¿Sabes que es el síndrome de hipertensión pulmonar persistente? La incidencia de HPPN es de 1.9 por cada 1.000 recién nacidos. Estos pacientes presentan numerosas complicaciones ante la aparición del síndrome.
La mortalidad derivada de la HPPN, varía según la causa subyacente, sin embargo se estima que en países desarrollados alcanza un 12% de los recién nacidos con esta afección y, en zonas en vías de desarrollo, crece hasta el 70%. Conoce en profundidad esta patología y aprende a detectarla y tratarla en este artículo.
Si solo dispones de unos segundos para leer este post, puedes leer las ideas más destacadas en este resumen:
- La HPPN se expresa como una hipoxemia severa resistente al tratamiento con una gran labilidad en la saturación arterial de O2 y en la PaO2
- Se presenta, comúnmente, asociada a patologías pulmonares como: síndrome de aspiración de meconio (50%), Neumonía/sepsis (20%), Síndrome de dificultad respiratoria (5%), Asfixia perinatal o Policitemia/hiperviscosidad (5%)
- La HPPN puede diagnosticarse empleando diferentes estrategias. Entre estos destaca el ecocardiograma, que se ha convertido en el método diagnóstico estándar. La organización mundial de la salud ha definido HPPN como una presión sistólica de la arteria pulmonar > 30 mmHg, correspondiente a una velocidad de regurgitación tricúspidea de 3 m/s medidos por ecocardiografía.
- El manejo inicial consiste en manipulación mínima y corregir los factores que favorecen la vasoconstricción como son la hipotermia, la hipoglucemia, la hipocalemia, la anemia y la hipovolemia. Dependiendo de la gravedad de la HPPN, será necesario el uso de surfactante pulmonar administrado por medio del método LISA, empleo de ventilación alveolar o soporte ventilatorio, el establecimiento de un tratamiento con óxido nítrico inhalado o la regulación del PDE5 con la utilización de un inhibidor como el sildenafilo.
Si tienes tiempo y quieres ampliar tu conocimiento, lee la entrada completa y comparte con nosotros tus inquietudes sobre la posible contaminación de la leche materna en las UCIN:
El síndrome de Hipertensión Pulmonar Persistente Neonatal (HPPN), también conocido como circulación fetal persistente, fue descrito por primera vez como “nacimiento inmaduro de la humanidad” por William Harvey en 1628 en su libro Exercitatio Anatomica De Motu Cordis et Sanguinis in Animalibus (1). Sin embargo, el síndrome paso desapercibido durante mucho tiempo, hasta la segunda mitad del siglo XIX.
En la década de 1960 varios investigadores lo redescubrieron. Benson (2) señaló en 1961 dos casos en los que “el conducto arterioso se encontró abierto con una dirección de flujo fetal desde la arteria pulmonar hacia la aorta”. También demostró que “el foramen oval en bebés que sufren de asfixia se mantenía permeable, a pesar de que no hubiese sufrido el debido proceso de obliteración o que se hubiera reabierto” (2).
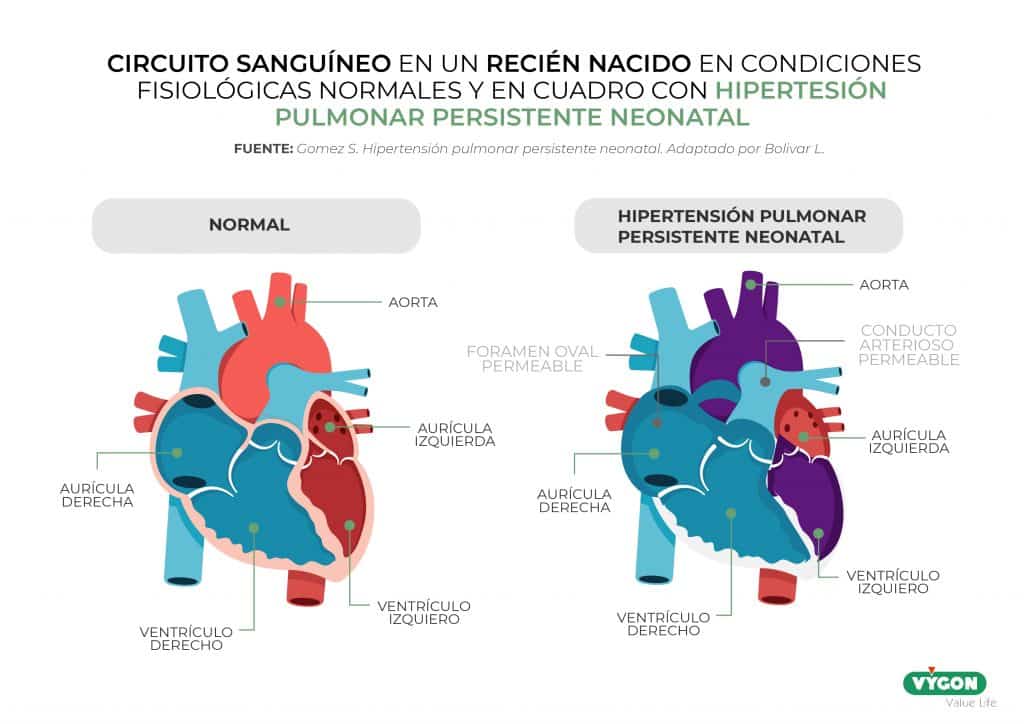
¿Qué es la hipertensión pulmonar persistente neonatal?
La HPPN no es una afección individual. Se trata de un conjunto de manifestaciones clínicas que puede acompañar a otras patológicas durante periodo neonatal. Clínicamente, la HPPN se expresa como una hipoxemia severa resistente al tratamiento con una gran labilidad en la saturación arterial de O2 y en la PaO2 (3).
Factores asociados a su aparición
La hipertensión se caracteriza por el incremento en la relación entre la resistencia vascular pulmonar (RVP) y la resistencia vascular sistémica (RVS), que resulta de vasoconstricción, remodelación estructural vascular pulmonar u obstrucción intravascular por hiperviscosidad u otros motivos.
Algunos estudios han encontrado asociación con el tabaquismo materno y el consumo de antiinflamatorios no esteroideos durante el embarazo (4).
La HPPN puede ocurrir sin enfermedad asociada del parénquima pulmonar (20%). Sin embargo, se presenta más comúnmente asociada a patologías pulmonares como:
- Síndrome de aspiración de meconio (50%)
- Neumonía/sepsis (20%)
- Síndrome de dificultad respiratoria (5%), y otras causas como
- Asfixia perinatal
- Policitemia/hiperviscosidad (5%) (5,6,7).
TE PUEDE INTERESAR
Valoración del patrón respiratorio del recién nacido: la escala de Silverman
¿Cómo identificar el síndrome de HPPN?
Si bien la presentación clínica de la HPPN es variable, sus características más clásicas son la hipoxemia, la labilidad, las variaciones espontaneas de la PaO2, y la sensibilidad a la alcalosis en un recién a nacido a término o a casi termino.
Además de la hipoxemia se pueden dar episodios de taquipnea y taquicardia y, en ocasiones, veces un soplo sistólico de regurgitación tricúspidea (9).
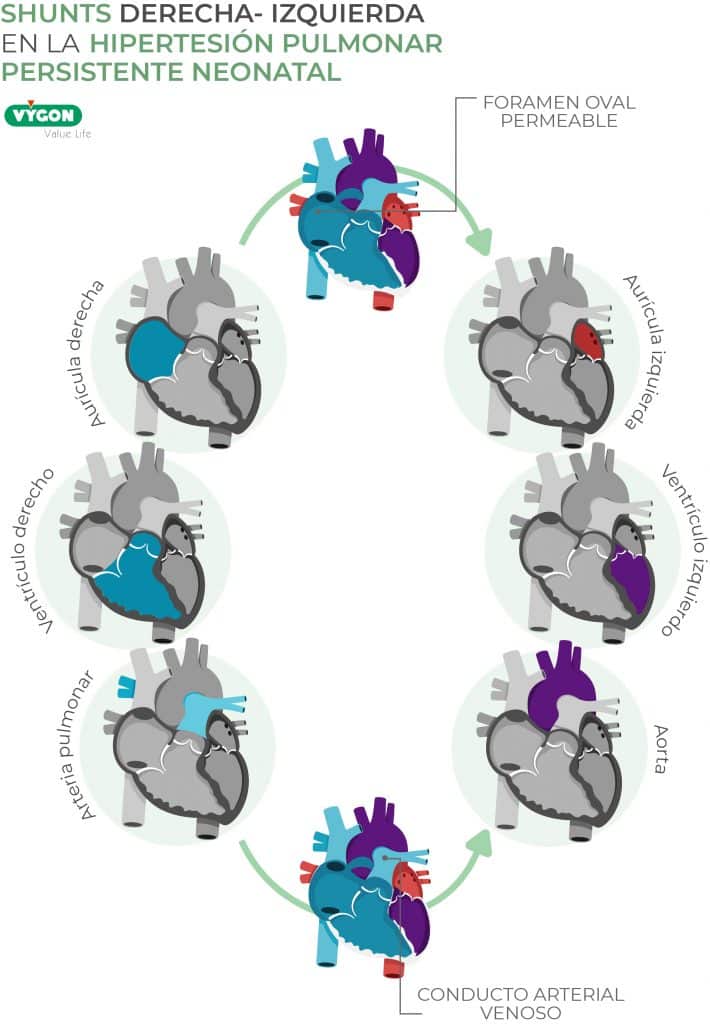
La ecocardiografía es muy útil para descartar cardiopatías congénitas y ocasionalmente para confirmar el grado de hipertensión pulmonar y derivación (shunt) de derecha a izquierda extrapulmonar (ya sea nivel ductal o del foramen oval) (9).
Diagnosticar la HPPN
Diagnóstico clínico
Los signos de dificultad respiratoria poco después del nacimiento son atribuibles a diferentes patologías pulmonares o simplemente a transición alterada a la vida extrauterina, sin embargo, cuando un recién nacido tiene dificultad respiratoria acompañada de oxigenación lábil e hipoxemia desproporcionadas al grado de patología pulmonar, debe sospecharse de HPPN (10-12).
Gradiente pre – post ductal
Esta prueba se realiza con el objetivo de establecer un diagnóstico presuntivo/hipotético de HPPN. El grado de oxigenación pre y post ductal, medido en forma simultánea por determinación de la PaO2 O SpO2 es útil para confirmar la presencia de shunt o cortocircuito de derecha a izquierda a nivel ductal que existe en el 50 a 60% de los RN con HPPN (8,9,11-13).
En estos casos los valores son más elevados en el territorio preductal (arteria radial derecha) que en el territorio postductal (arterias umbilicales o de extremidades inferiores) (14,15).
Con PaO2 bajas (30-55 mmHg) una diferencia pre – post ductal de 10 mmHg es muy significativa. Con PaO2 altas (80-150 mmHg) la diferencia tiene que ser mayor (15-20 mmHg o más) para asumir que hay un shunt importante de derecha a izquierda. Para la SpO2 la interpretación es similar, con una diferencia mayor o igual al 3%.
Es necesario recordar que una prueba negativa no excluye el diagnóstico, pues cuando hay un cortocircuito significativo de derecha a izquierda a nivel de foramen oval o cuando hay hipoflujo pulmonar sin shunt, no se produce esta diferencia pre – post ductal (4,16,17).
Ecocardiograma
La organización mundial de la salud ha definido HPPN como una presión sistólica de la arteria pulmonar > 30 mmHg, correspondiente a una velocidad de regurgitación tricúspidea de 3 m/s medidos por ecocardiografía (ECO).
Este método de diagnóstico se ha considerado el estándar de oro, ya que determina la afectación cardíaca, descarta alteraciones estructurales y evalúa la respuesta al tratamiento y al pronóstico de forma no invasiva (4,16,17).
La técnica Doppler es un excelente complemento no invasivo para estimar la presión de la arteria pulmonar que se detecta en más del 90% de los casos. Con Doppler es posible determinar la severidad de la HPPN y su respuesta al tratamiento mediante la regurgitación tricúspidea y la documentación de los cortoscircuitos extra pulmonares (18,19).
Gases Sanguíneos Arteriales
Lo primero para tener en cuenta es tomar la muestra de sangre arterial bajo un protocolo de mínima manipulación y con el equipo ideal. Se recomienda usar el equipo fidedigno para minimizar el trauma y la hemolisis.
En el análisis se observará hipoxia progresiva que conduce a hipoxemia persistente con PaO2 menor de 50 mmHg a pesar de FiO2 al 100%. La PaO2 puede disminuir de 100 a 40 mmHg en cuestión de minutos y puede desarrollarse acidosis mixta con pH menor de 7.25. Es necesario un monitoreo cuidadoso de los gases en la sangre arterial, para calcular el gradiente alveolo-arterial del oxígeno (AaDO2) y el índice de oxigenación (IO) y, así, valorar la gravedad en estos casos. Un IO mayor de 25 o la AaDO2 mayor de 610 mmHg, indican una enfermedad grave (20,21).

¿Cómo manejar la HPPN?
El manejo inicial consiste en manipulación mínima y corregir los factores que favorecen la vasoconstricción como son la hipotermia, la hipoglucemia, la hipocalemia, la anemia y la hipovolemia.

TAMBIÉN TE PUEDE INTERESAR
El uso de agentes alcalinizantes es controvertido. Se debe optimizar la función cardiaca según necesidad con expansores de volumen y agentes inotrópicos (dobutamina, dopamina, milrinona) (22,23).
La gravedad de la HPPN puede variar desde una hipoxemia leve con una mínima dificultad respiratoria hasta una hipoxemia grave e inestabilidad cardiopulmonar que requiera de cuidados intensivos y empleo de catéteres centrales de inserción periférica neonatales, que permitan la administración simultanea de soporte hídrico, nutricional, inotrópico y además la administración del tratamiento farmacológico propio de la patología.

Los bebés con HPPN requieren cuidados de apoyo, incluyendo una temperatura óptima y apoyo nutricional, evitar el estrés y el manejo con sedación y analgesia según sea necesario (24).
Los casos leves de HPPN con mínima o nula dificultad respiratoria pueden detectarse en la sala de neonatos tras un episodio de desaturación o por una baja saturación de oxígeno postductal detectada en el cribado de cardiopatías congénitas críticas. Estos bebés pueden ser tratados con cuidados de apoyo y suplementos de oxígeno.
Es importante una vigilancia estrecha porque algunos de estos bebés pueden deteriorarse rápidamente y requerir ventilación no invasiva o intubación y ventilación mecánica (25).
Administración de Surfactante
Se ha demostrado que el uso de surfactante pulmonar administrado por medio del método LISA de manera prematura en bebes con HPPN secundaria a SAM o neumonía mejora la oxigenación y disminuye la necesidad de uso de circulación por membrana extracorpórea (ECMO) (26).
Ventilación alveolar y soporte ventilatorio
Se ha reportado que entre el 10-20% de pacientes con HPPN leve o moderada requieren solo CPAP, el 25% requieren ventilación mecánica convencional (VMC) y un tercio requieren ventilación de alta frecuencia (VAF) (27, 28).
La ventilación mecánica convencional (VMC) como terapia de esta condición debe ser “anticipatoria” y tiene la finalidad de conseguir el máximo reclutamiento alveolar para lograr un volumen pulmonar optimo minimizando el riesgo de injuria.
El tener volúmenes pulmonares por encima o por debajo de la capacidad residual funcional empeora la hipoxemia y aumenta la RVP. La sobre distensión del pulmón empeora la hipertensión pulmonar, ya que el alveolo sobre distendido comprime los capilares y las pequeñas arteriolas y aumenta la RVP. La VMC con presiones excesivas también puede producir una complicación aguda pulmonar, edema pulmonar, disminución de la complacencia e inflamación pulmonar (3).
La VAF emplea volúmenes corrientes muy pequeños (menores que el espacio muerto anatómico), en frecuencias respiratorias supra fisiológicas (superiores a 150 respiraciones/minuto), permitiendo de esta forma mantener una ventilación adecuada (29).
La VAF reduce la necesidad de ECMO en pacientes con HPPN grave, en recién nacidos con HPPN que requieren aumentar demasiado las presiones o los parámetros del ventilador mecánico convencional para mantener un adecuado intercambio gaseoso es necesario considerar la VAF para reducir el barotrauma. Cuando se utiliza VAF los objetivos son:
- Optimizar la expansión pulmonar y la capacidad residual funcional
- Evitar la sobredistensión (30).
Oxido Nítrico Inhalado
El óxido nítrico inhalado (iNO) es el tratamiento más obvio, así como el más estudiado y aceptado para la HPPN. Actúa localmente como vasodilatador pulmonar.
El iNO se considera eficaz y seguro para su uso en lactantes con HPPN, excepto en aquellos con hernia diafragmática congénita asociada (31). Sin embargo, además de no reducir la mortalidad de la HPPN y de ser una intervención costosa, el 40% de los neonatos con HPPN no responden al iNO, y algunos de ellos experimentan además un rebote de PH, muy probablemente debido a la supresión de la producción endógena de NO (32).
Inhibidor de la PDE5
La PDE5 es un regulador clave de la reactividad vascular pulmonar de los recién nacidos, y su inhibición conduce a la vasodilatación. Por ello, los inhibidores de la PDE5, principalmente el sildenafilo, se estudian actualmente como tratamiento de la HPPN (33).
En general, el sildenafilo utilizado como tratamiento de la HPPN tiene potencial para reducir la mortalidad y mejorar la oxigenación en estos lactantes. Sin embargo, hasta la fecha, los ensayos disponibles son limitados y carecen de calidad de las pruebas, debido a los pequeños tamaños de las muestras y a las características metodológicas poco fiables.
No dudes en comunicarnos tus dudas y dejarnos un comentario.
BIBLIOGRAFÍA
- D’cunha C, Sankaran K. Persistent fetal circulation. Paediatr Child Health. 2001 Dec; 6(10): 744–750. (Consultado el 15/05/2021). Disponible en: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2805987/
- Benson, P. Changes in the Circulation at Birth. Developmental Medicine & Child Neurology, 1961 3(5), 426–428. doi:10.1111/j.1469-8749.1961.tb10389.x. (Consultado el 15/05/2021). Disponible en: sci-hub.se/10.1111/j.1469-8749.1961.tb10389.x
- Baquero H, Sola A. Patologías con Hipoflujo Pulmonar. En: Sola A. Cuidados Neonatales: Descubriendo la vida de un recién nacido. Tomo II. Ed. Distribuna, Edimed. 2011 978-990.
- Sergio G, Sola A, Lourdes L. Recomendaciones del consenso clínico de SIBEN para la hipertensión pulmonar persistente del recién nacido. Neoreviews. 2017 May; 18 (5): 327-344. (Consultado el 15/06/2021). Disponible en: https://neoreviews.aappublications.org/content/neoreviews/18/5/e327.full.pdf
- Walsh-Sukys M, Tyson J, Wright L, et al. Persistent pulmonary hypertension of the newborn in the era before nitric oxide: practice variation and outcomes. Pediatrics. 2000;105(1 pt 1):14–20.
- Stayer S, Liu Y. Pulmonary hypertension of the newborn. Best Pract Res Clin Anaesthesiol. 2010;24(3):375–386.
- Larrue B, Jaillard S, Lorthioir M, et al. Pulmonary vascular effects of sildenafil on the development of chronic pulmonary hypertension in the ovine fetus. Am J Physiol Lung Cell Mol Physiol. 2005;288(6): L1193–L1200.
- Sola A, Porto R. Hipertensión pulmonar persistente en el recién nacido. En: Sola A, Urman J. Cuidados especiales del feto y recién nacido. Ed. Científica Interamericana. 2001: 1003-19.
- Baquero H, Sola A. Patologías con Hipoflujo Pulmonar. En: Sola A. Cuidados Neonatales: Descubriendo la vida de un recién nacido. Tomo II. Ed. Distribuna, Edimed. 2011: 985.
- Silvera F, Mele A, Costas M. Hipertensión pulmonar e hipoxemia grave en recién nacidos. Arch Pediatr Urug. 2007;78(4).
- Sola A Cuidados Neonatales: descubriendo la vida de un recién nacido enfermo. 1st ed. Buenos Aires, Argentina: Buenos Aires Edimed; 2011:987–988.
- Diaz G, Sandoval N, Velez J, eds. Cardiologia Pediátrica. Bogotá, Columbia: McGraw-Hill Interamericana; 2003:797–802.
- Bland R. Formation on fetal lung liquid and its removal near birth. In: Polin RA, Fox WW, eds. Fetal and Neonatal Physiology. Philadelphia, PA: WB Saunders; 1997:782–789.
- Klinger G, Beyene J, Shah P, Perlman M. Do hyperoxaemia and hypocapnia add to the risk of brain injury after intrapartum asphyxia? Arch Dis Child Fetal Neonatal Ed. 2005;90(1):F49–F52.
- Lozano C, Hernandez R, Leboreiro J, Bernardez Z, Vidaña D. Saturación pre y postductal en recién nacidos sanos de la Ciudad de México. Acta Médica Grupo Ángeles. 2020; 18 (2): 146-150. (Consultado el 20/06/2021). Disponible en: https://www.medigraphic.com/pdfs/actmed/am-2020/am202e.pdf
- Victoria-Oliva G, Mojarro-Rios J, Alva-Espinosa C, Villasis-Keever MA, Labarthe-Cabrera J, Arellanos-Penago M, Velasco-Jímenez S. Ecocardiografía Doppler en recién nacidos con riesgo de hipertensión arterial pulmonar. Rev Mex Cardiol. 1996;7(1):25–31.
- Parlakay AO, Karagöz T, Ozkutlu S, Ozen S, Alehan D. Evaluation of diagnostic accuracy of portable echocardiography in newborns Anadolu Kardiyol Derg. 2011; 11(7):627-32 (ISSN: 1308-0032).
- Silvera F, Mele A, Costas M. Hipertensión pulmonar e hipoxemia grave en recién nacidos. Arch Pediatr Urug. 2007;78(4).
- Howard L, Grapsa J, Dawson D, et al. Echocardiographic assessment of pulmonary hypertension: standard operating procedure. Eur Respir Rev. 2012;21(125):239–248
- Gomella T. Persistent pulmonary hypertension of the newborn. In: Gomella TL, Cunningham MD. Neonatology. Management, procedures, on call problems, diseases and drugs. 5th ed. McGraw-Hill. 2004: 364-370.
- Whitsett J, Pryhuber G, Rice W, Warner B, Wert S. Persistent pulmonary hypertension of the newborn. In: Avery’s MacDonald MG, Mullett MD, Seshia MMK. Neonatology: pathophysiology and management of the newborn. 6th ed. Lippincott Williams & Wilkins. 2005: 565-9.
- Arias D, Narvaez C. Guía de práctica clínica Atención al recién nacido con hipertensión pulmonar persistente. repert med cir. 2016;25(4):219–227. (Consultado el 31/06/2021). Disponible en: https://www.fucsalud.edu.co/sites/default/files/2017-03/08-Guia-practica-clinicaAtencion-recien-nacido.pdf
- Sharma V, Berkelhamer S, Lakshminrusimha S. Persistent pulmonary hypertension of the newborn. Matern Health Neonatol Perinatol. 2015 Jun 3;1:14. doi: 10.1186/s40748-015-0015-4. PMID: 27057331; PMCID: PMC4823682. (Consultado el 31/06/2021). Disponible en: https://pubmed.ncbi.nlm.nih.gov/27057331/
- Laksminrusimha S, Keszler M. Persistent Pulmonary Hypertension of the Newborn. NeoReviews December 2015, 16 (12) e680-e692; DOI: https://doi.org/10.1542/neo.16-12-e680. (Consultado el 01/03/2021). Disponible en: https://neoreviews.aappublications.org/content/16/12/e680
- Manja V, Mathew B, Carrion V. Critical congenital heart disease screening by pulse oximetry in a neonatal intensive care unit. J Perinatol. 2014.
- Walsh M, Fanaroff J. Meconium stained fluid: Approach to the mother and the baby. Clin Perinatol. 2007;34:653–65.
- Singh B, Clark R, Powers R, Spitzer A. Meconium aspiration syndrome remains a significant problem in the NICU: outcomes and treatment patterns in term neonates admitted for intensive care during a ten-year period. J Perinatol. 2009;29(7):497–503.
- Wiswell T, Gannon C, Jacob J, et al. Delivery room management of the apparently vigorous meconium-stained neonate: results of the multicenter, international collaborative trial. Pediatrics. 2000;105(1 pt 1):1–7
- Castillo F, Elorza D, Gutierrez A, Moreno J, Bustos G, Gresa M, Miracle X, Et al. Recomendaciones para la asistencia respiratoria en el recién nacido (IV). Ventilación de alta frecuencia, ex-utero intrapartum treatment (EXIT), oxigenador de membrana extracorpórea (ECMO). ASOCIACIÓN ESPAÑOLA DE PEDIATRÍA. 2017. Noviembre. Vol. 87. Núm. 5. páginas 295.e1-295.e7. DOI: 10.1016/j.anpedi.2017.04.003. (Consultado el 01/07/2021). Disponible en: https://www.analesdepediatria.org/es-recomendaciones-asistencia-respiratoria-el-recien-articulo-S1695403317301777.
- Hansmann G. Persistent pulmonary hypertension of the newborn (PPHN). Neonatal Emergencies: A Practical Guide for Resuscitation, Transport and Critical Care, ed. Georg Hansmann. Published by Cambridge University Press. (Consultado el 04/07/2021). Disponible en: https://www.cambridge.org/core/terms. https://doi.org/10.1017/CBO9781139010467.057.
- Barrington K, Finer N, Pennaforte T, Altit G. Nitric oxide for respiratory failure in infants born at or near term. Cochrane Database Syst Rev. (2017) 1:CD000399. doi: 10.1002/14651858.CD000399.pub3
- Lakshminrusimha S, Mathew B, Leach CL. Pharmacologic strategies in neonatal pulmonary hypertension other than nitric oxide. Semin Perinatol. (2016) 40:160–73. doi: 10.1053/j.semperi.2015.12.004
- Rubin LJ, Badesch DB, Fleming TR, Galiè N, Simonneau G, Ghofrani HA, et al. Long-term treatment with sildenafil citrate in pulmonary arterial hypertension: the SUPER-2 study. Chest. (2011) 140:1274–83. doi: 10.1378/chest.10-0969.




0 comentarios