Trabajar como enfermera en Hospital de Día Oncológico (HDO) supone seguir unas estrictas medidas de seguridad, como la purga del equipo de infusión tras quimioterapia, cuando se administra tratamientos citostáticos a los pacientes.
Tanto en la recepción de la bolsa de tratamiento, la preparación de los dispositivos y la administración, es necesario seguir un protocolo claro para minimizar los riesgos.
Respecto a la parte post-administración, muchas guías internacionales como es el caso de las guías australianas Guidelines for the Safe Prescribing, Supply and Administration of Cancer Chemotherapy(1), indican lo siguiente:
“Después de la administración, la línea intravenosa debe ser purgada con un volumen suficiente de solución compatible con el fármaco.”
Pero ¿por qué se tiene que lavar la línea de infusión? ¿Es realmente eficaz este lavado?
Puntos claves del artículo:
- dentro del procedimiento de administración de citostáticos, la purga de los fármacos es un paso importante para reducir el riesgo de exposición
- la purga por gravedad no es eficiente, en cuanto menos dura, menos efecto tiene
- la limpieza con bolo continuo tampoco es lava correctamente y supone más riesgo de infección
- el lavado con técnica push-pause (bolos intermitentes) ha demostrado ser la más eficiente
- aun así no elimina al 100% el riesgo de exposición en el momento de quitar los equipos de infusión y es necesario usar sistemas cerrados especialmente diseñados para ello.
¿CÓMO SE EFECTÚA LA ADMINISTRACIÓN DE QUIMIOTERAPIA EN HDO?
Es importante recordar que enfermería sigue siendo un grupo de riesgo respecto a la manipulación de citostáticos y que el tiempo de exposición es clave.
En el estudio Evaluation of genotoxicity induced by exposure to antineoplastic drugs in lymphocytes of oncology nurses and pharmacists(2), que compara el grupo de farmacéuticos y el grupo de enfermería respecto a las consecuencias de esta exposición (antigüedad de entre 2 y 20 años), llega a las conclusiones siguientes:
“Había una diferencia en cuanto a los años de exposición entre farmacéuticos y enfermeras, siendo más alto para el último grupo, que también tenía niveles más altos de daño cromosómico y linfocitos aberrantes”.
El estudio infiere que la razón de la diferencia entre enfermeras y farmacéuticos se debe al hecho de que este último adopta una protección más estricta cuando manejando drogas antineoplásicas, con guantes, máscaras y batas, mientras que las enfermeras sólo se ponen guantes.
Los riesgos de exposición por aerosoles son especialmente altos en el momento de la desconexión. Por esta razón, después de su administración, se recomienda no desconectar las bolsas de citostáticos cuando no se usa sistemas especialmente diseñados para ellos (SCTM). Y consecuentemente se tiene que proceder al lavado del equipo de perfusión y del acceso vascular, con suero fisiológico (excepto en caso de incompatibilidades).
¿Cuáles son los pasos en la administración de una quimioterapia?
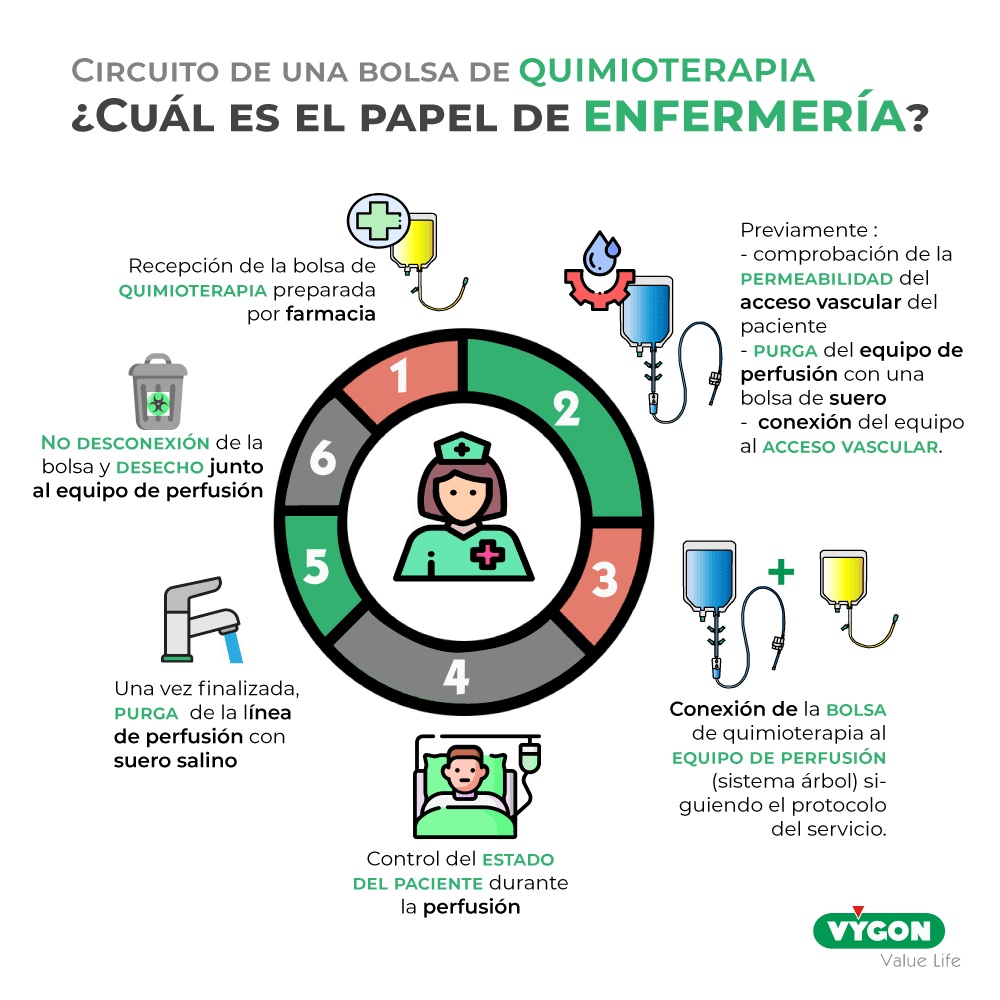
Este proceso se puede llegar a repetir muchas veces en un día de trabajo. En función del tratamiento que vaya a recibir el enfermo, se puede conectar una o varias bolsas en una misma sesión. La inmensa mayoría de los protocolos indican que es necesario purgar entre 2 perfusiones de citostáticos.
El objetivo de esta purga es poder eliminar los restos de citostáticos que puede contener el equipo de perfusión y el catéter para minimizar el riesgo de exposición.
¿Pero qué dice la literatura sobre la eficiencia de este lavado?
¿Qué datos tenemos sobre la eficacia de la purga del equipo de infusión tras la administración de quimioterapia?
Existen varios métodos para purgar un acceso vascular. Entre ellos se encuentran la purga continua por gravedad (con bolsa de suero), el lavado continuo con jeringa y la limpieza pulsada con jeringa. Cada técnica tiene indicaciones específicas según el tipo de acceso y la situación clínica.
En el caso de una administración de citostáticos, aunque el sistema de gotero se abra completamente para lavar el equipo de perfusión, así como el catéter con el máximo flujo posible por gravedad, varios estudios han demostrado que su acción es limitada.
En el año 2012, Guiffant et al.(3) han investigado sobre estos 3 métodos para determinar cual de ellos era el más eficiente. Los resultados demuestran que una infusión continua de suero como es el caso de una bolsa por gravedad (guarda vena) es insuficiente y en cuanto menos tiempo está en marcha, menos eficiente es:
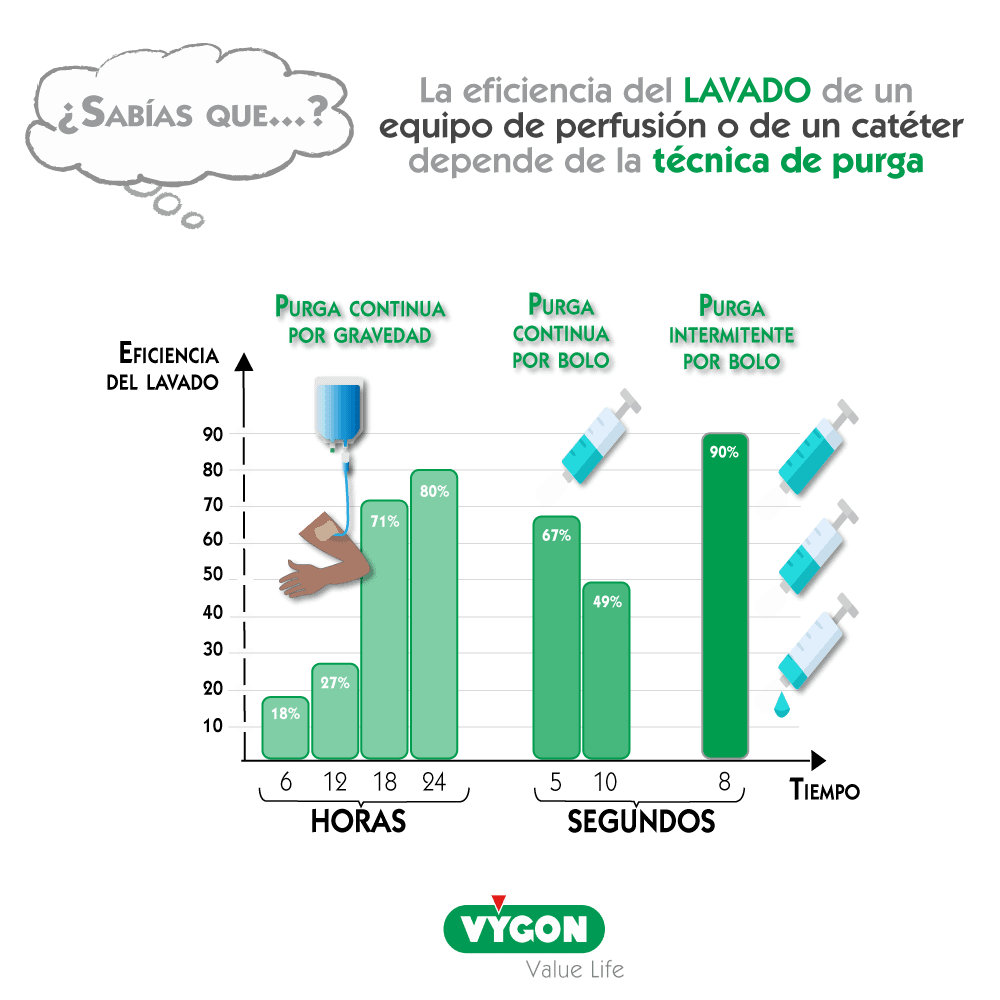
Además, el mismo equipo de investigación demostró 2 años después, que también tiene una incidencia sobre la colonización bacteriana: los catéteres que reciben un lavado continuo en lugar de pulsado, tienen una tasa de contaminación más elevada(4).
Varios estudios dejan claro que la mejor manera de lavar un acceso vascular (de cualquier tipo) es efectuando una purga pulsada (push-pause).
Las 2 variables fundamentales para ello son el flujo y la duración de las pausas (0.4s).
El manual sobre PICC/midline de GAVeCeLT(5) recomienda bolos de 2-3ml para aplicar correctamente esta técnica y recuerda que la purga se tiene que hacer antes y después de cada perfusión.
“La eliminación completa de los citotóxicos de una línea de infusión es un objetivo poco realista. Incluso cuando se lava, el equipo de infusión debe considerarse una fuente de contaminación citotóxica.”
Este estudio destaca la importancia de usar un dispositivo de sistema cerrado (SCTM) al final de la línea de infusión. El volumen de lavado óptimo debe ser suficiente para administrar la dosis completa con una concentración residual mínima. No se busca una línea completamente libre de residuos.
Hay poca bibliografía sobre este tema, por lo que se necesita más investigación. Sin embargo, los primeros resultados sugieren la importancia de adoptar medidas eficaces para reducir los residuos de citostáticos en las líneas de perfusión.
¿QUÉ SOLUCIONES EXISTEN?
Como dicho anteriormente el lugar más propicio a la liberación de vapores o aerosoles son las conexiones. Durante la administración, pueden ser sometidas a la agresividad de los fármacos y a la fuerza de la rosca, 2 factores que pueden provocar microfisuras.
Además, si no es posible purgar correctamente el equipo de perfusión y el prolongador del acceso vascular, el momento de la desconexión representa un alto riesgo.
Por esta razón como indican Bartel(7) y Lancharro(8) en sus estudios, los SCTM son imprescindibles para minimizar el riesgo de exposición, de contaminación ambiental y personal que existe en una unidad de administración como HDO.
El SCTM, provisto de un sistema de conexión específico, garantiza que durante la perfusión las conexiones entre dispositivos se mantengan seguras. Además, en el momento de la desconexión, el cierre del sistema evita la liberación de vapores o gotas.
Es importante que enfermería pueda tener acceso a este tipo de recursos para poder protegerse de una manera adecuada. Para ello, es fundamental, según Eisenberg(9), involucrar al personal de enfermería en el proceso de selección del SCTM con farmacia, a fin de elegir el que mejor se adapte a sus prácticas.

bibliografía





0 comentarios