Estás ante un paciente crítico. Gasto cardíaco dentro de rango, presión arterial aceptable, retorno venoso aparentemente adecuado… pero algo no cuadra. El paciente no mejora.
Y es que, aunque lo que puedes medir te dice que todo va bien, puede que la perfusión celular siga comprometida. Esta es una de las grandes paradojas en el manejo hemodinámico: tener buena presión no significa tener buena perfusión.
La microcirculación puede aportarnos mucha información valiosa, si sabemos cómo aprovecharla.
Por si no tienes tiempo para leerlo, te resumimos el artículo en un minuto
- La monitorización hemodinámica tradicional se ha centrado en la macrocirculación —presión arterial, gasto cardíaco, retorno venoso—, pero estos parámetros no siempre reflejan el estado real de la perfusión tisular.
- La microcirculación, como vía final para el aporte de oxígeno y nutrientes a las células, representa un eslabón crítico y frecuentemente invisible.
- La disociación entre macro y microcirculación puede comprometer la toma de decisiones, incluso cuando los valores globales parecen “normales”.
- Este artículo resume parte de la ponencia del Dr. Wong, explicando por qué no basta con optimizar la macrocirculación, analiza las limitaciones de los enfoques actuales, y presenta las claves para una monitorización más coherente e integrada, centrada en lo que realmente importa: la perfusión efectiva a nivel celular.
Una mirada más profunda: el límite de la hemodinámica clásica
Durante décadas, la medicina intensiva se ha centrado en valorar la macrocirculación: perfusión tisular, presión arterial, flujo sanguíneo. Es lo que podemos medir con mayor facilidad. Sin embargo, las evidencias han demostrado que estos indicadores no reflejan necesariamente una perfusión tisular adecuada.
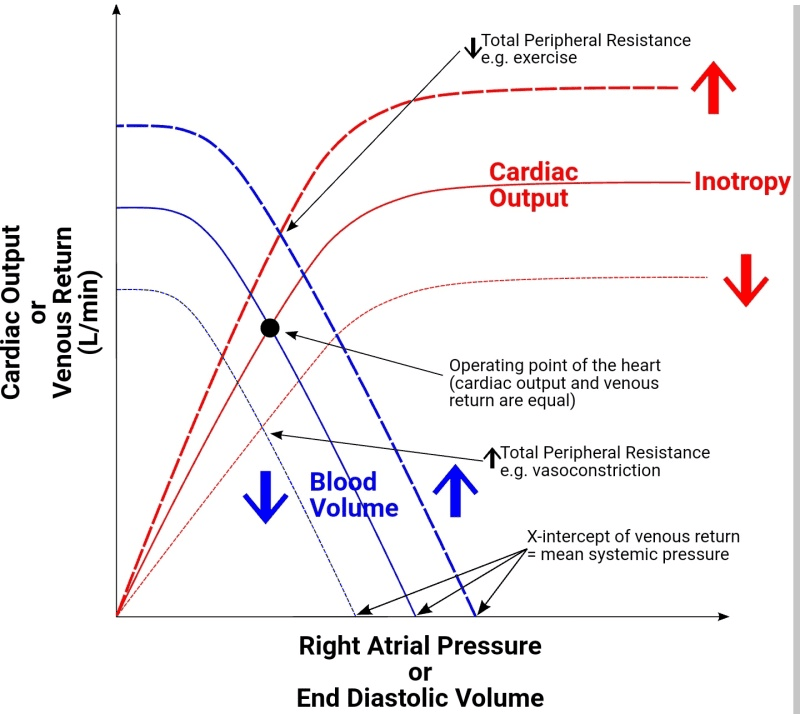
El objetivo real de la hemodinámica debería ser asegurar que cada célula reciba suficiente oxígeno y lo utilice de forma eficaz. Pero para eso, necesitamos mirar más allá de lo que vemos en el monitor.
El verdadero campo de batalla: la microcirculación
La perfusión no se decide en la arteria femoral ni en el gasto cardíaco: se decide en la célula. Ahí es donde el oxígeno debe llegar, liberarse y ser utilizado. Y ese proceso ocurre en el terreno menos visible: la microcirculación.
La microcirculación puede estar alterada incluso en pacientes hemodinámicamente estables a nivel macro. En otras palabras: puede haber disfunción celular sin alteración de los parámetros tradicionales. De ahí nace la necesidad de monitorizar más allá de la macrocirculación.
¿Respondedor o tolerante? Redefiniendo la fluidoterapia
En los últimos años, el concepto de “tolerancia a fluidos” ha cobrado fuerza. Hasta ahora, hemos guiado el tratamiento por la respuesta hemodinámica a la administración de volumen. Pero hoy sabemos que responder no implica necesariamente que el paciente necesite ese volumen.
La decisión ya no debería basarse únicamente en si hay respuesta, sino también en si existe tolerancia. Esta visión permite evitar la sobrecarga y ajustar el tratamiento de forma más individualizada y fisiológica.
Estudios como “Fluid responsiveness and venous congestion: unraveling the nuances of fluid status” o “Coexistence of a fluid responsive state and venous congestion signals in critically ill patients: a multicenter observational proof-of-concept study” indican como el estado de respuesta a fluidos puede coexistir con el estado de intolerancia. La intolerancia y la respuesta a fluidos no son polos puestos, sino que muchas ocasiones se conectan, es decir, existe un “área controversial” y unos parámetros macrocirculatorios no garantizan una correcta perfusión microcirculatoria.
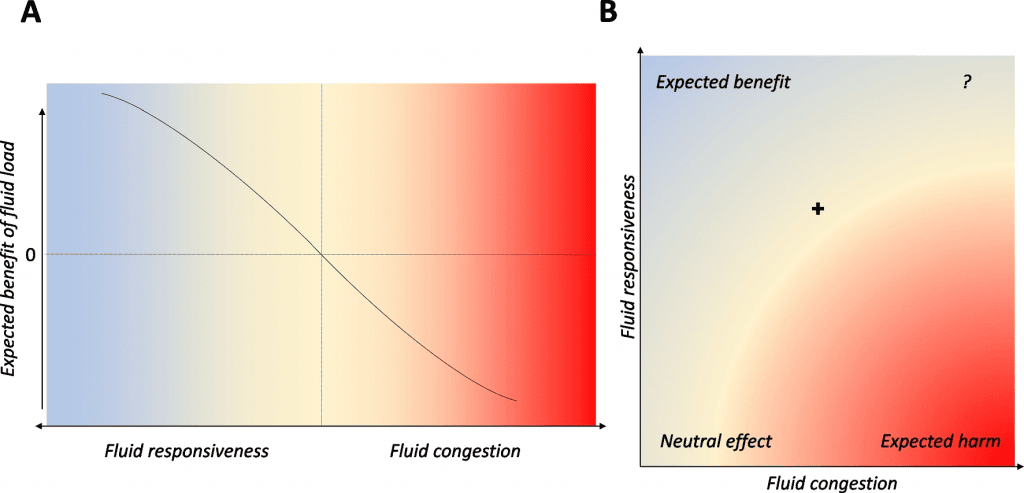
Medir lo invisible: cómo monitorizar la microcirculación
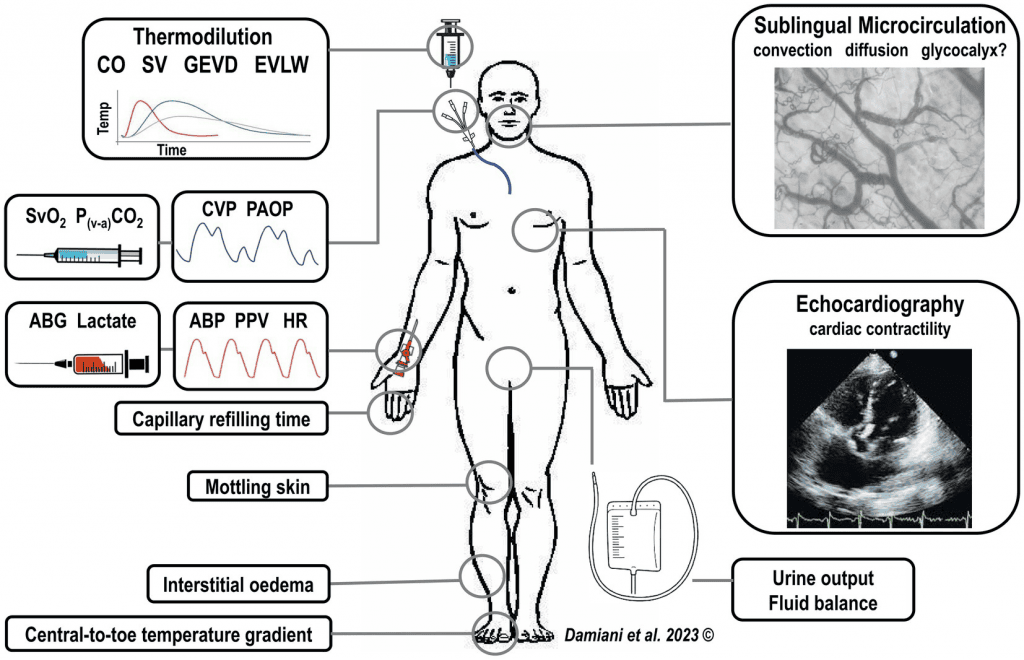
Una de las grandes limitaciones actuales es que no existe una herramienta estandarizada para evaluar la microcirculación. Sin embargo, disponemos de parámetros y dispositivos que permiten acercarnos a esa realidad, como:
- Videocapilaroscopia del lecho ungueal
- Tiempo de relleno capilar
- Ecografía con contraste (CEUS: contrast enhanced ultrasound)
- Gap Veno-arterial PCO2
Con ellos podemos inferir el estado de la microcirculación y tomar decisiones más informadas.
Coherencia hemodinámica: cuando macro y micro van de la mano
El objetivo terapéutico debe ser lograr la coherencia hemodinámica: que las intervenciones que realizamos a nivel macrocirculatorio generen una mejoría real en la perfusión celular.
En la práctica, esto implica adaptar los tratamientos según el estado evolutivo del paciente, porque:
- En las fases tempranas del shock, suele haber coherencia entre macro y micro.
- En fases avanzadas, puede haber disociación: la presión mejora, pero la microcirculación no.
Este enfoque promueve un tratamiento más preciso, centrado no en los valores, sino en el beneficio real para la célula.
Desafíos actuales
- Disociación entre microcirculación y macrocirculación: la disfunción de la microcirculación puede ocurrir incluso cuando la macrocirculación es normal. La microcirculación es el sitio principal para el intercambio de oxígeno entre sangre y tejidos, y puede ser interrumpido por muchos factores.
- La optimización de la macrocirculación puede no mejorar la perfusión tisular si la microcirculación está alterada
- Sobre-optimización de la macrocirculación: puede llevar a sobrecarga de fluidos o abuso de vasopresores, lo que podría dañar la oxigenación de los tejidos
- Relaciones inciertas entre la presión sanguínea y la microcirculación: la relación óptima sigue siendo desconocida
- Falta de métodos fiables para medir la oxigenación regional de los tejidos.
El futuro de la terapia hemodinámica es individualizado
El concepto de monitorización hemodinámica personalizada marca el futuro de los cuidados intensivos. El objetivo ya no es solo corregir los valores, sino optimizar la perfusión celular de cada paciente, en cada momento.
Y para lograrlo, necesitamos integrar diferentes herramientas, apoyarnos en en algoritmos y protocolos que nos aporten cierta perspectiva microcirculatoria y concordancia entre macro-micro circulación.
Actualmente no existe un único dispositivo que nos aporte una respuesta universal. No hay un gold standard. Cada paciente es distinto y va evolucionando y cada dispositivo nos aportará diferente información valiosa que debemos saber interpretar.
Claves para llevar a la práctica
- La presión no es suficiente: no confundas estabilidad con perfusión.
- Evalúa siempre la respuesta y la tolerancia a los fluidos.
- Utiliza herramientas disponibles para explorar la microcirculación.
- Busca la coherencia hemodinámica como objetivo clínico.
- Personaliza el tratamiento según la fase evolutiva del shock.
¿Quieres seguir profundizando en hemodinámica avanzada? Entonces no te pierdas otras ponencias del Dr. Wong accediendo a VYHEMDAYS opción bronce.
Bibliografía
Damiani, E., et al. (2023). Microcirculation-guided resuscitation in sepsis: the next frontier? Sec. Intensive Care Medicine and Anesthesiology (10). https://doi.org/10.3389/fmed.2023.1212321
Joseph, A., et al. Fluid responsiveness and venous congestion: unraveling the nuances of fluid status. Crit Care 28, 140 (2024). https://doi.org/10.1186/s13054-024-04930-2
Muñoz, F., et al. (2024). Coexistence of a fluid responsive state and venous congestion signals in critically ill patients: a multicenter observational proof-of-concept study. Critical care (London, England), 28(1), 52. https://doi.org/10.1186/s13054-024-04834-1





Como mejoro la microcirculacion cardíaca?
Buenas José Carlos,
En este artículo encuentra una pequeña explicación de la ponencia. Si quiere saber más, por favor, consulte la bibliografía mencionada por el doctor que encontrará al final del artículo.