En pacientes con hipovolemia grave o shock hipovolémico, el retraso en la fluidoterapia puede provocar una lesión isquémica y un shock irreversible desencadenando un fallo multiorgánico, por ello es muy importante contar con información hemodinámica en tiempo real.3
¿Qué encontrarás en este artículo?
En este artículo conoceremos dos claves para identificar los primeros indicios de hipovolemia, y en caso de que esta se produzca, actuar precozmente:
1. Fluidoterapia guiada por objetivos.
La terapia guiada por objetivos (GDT) permite un uso más adecuado de los fluidos, vasopresores e inotrópicos y, por tanto, ofrece un mejor pronóstico y una recuperación más rápida.
2. Sistema de monitorización y parámetros hemodinámicos importantes.
La hipovolemia requiere una actuación inmediata para evitar riesgos que pongan en peligro la vida del paciente, por ello nuestro sistema debería mostrar los parámetros hemodinámicos en tiempo real, permitiéndonos identificar cualquier alteración en el estado del paciente y guiar la terapia. En estos pacientes, además de los parámetros clásicos de gasto cardíaco (GC), volumen sistólico (VS) o parámetros de presión, también son muy útiles la variación de la presión del pulso (PPV), la variación del volumen sistólico (SVV), elastancia arterial (Ea), eficiencia del ciclo cardíaco (CCE).
Las complicaciones intraoperatorias y postoperatorias en pacientes quirúrgicos de alto riesgo constituyen una de las principales causas de recuperación prolongada y supervivencia, además representan una proporción importante de los ingresos en UCI.1
En 2008 se estimó que se realizaron alrededor de 230 millones de procedimientos quirúrgicos en todo el mundo, y un número significativo de estos pacientes tenían riesgo de complicaciones intraoperatorias o postoperatorias. A pesar de que solo un 15% de los procedimientos se realizaron en pacientes de alto riesgo, estos pacientes representaron el 80% de las muertes. 1
Por ello, todas las actividades y procedimientos enfocados reducir estos riesgos contribuirán, no solo a una mayor seguridad del paciente, sino también reducirá los costes de la atención médica. 1
En críticos y durante una cirugía, el paciente puede presentar cambios hemodinámicos inesperados que sucedan de un momento a otro. La causa más común de descompensación cardiovascular en el quirófano es la hipovolemia. 2
Causas de shock en el quirófano
Los estados de shock tienen múltiples causas, pero todos dan como resultado hipoperfusión a órganos vitales, lo cual puede provocar insuficiencia orgánica y muerte si no se maneja de manera rápida y adecuada.5
El shock requiere tratamiento inmediato ya que puede empeorar muy rápidamente. Tal es la gravedad que 1 de cada 5 personas en shock muere. 6
La insuficiencia cardiovascular, o shock, puede ser causada por:
- Problemas cardíacos: Shock cardiogénico. 6
- Poco volumen de sangre y líquidos: Shock hipovolémico hemorrágico y no hemorrágico. 6
- Reacción alérgica: Shock anafiláctico. 6
- Infección: Shock séptico. 6
- Daño al sistema nervioso: Shock neurogénico. 6
Si se descompensa el shock, la presión arterial media o el gasto cardíaco serán inadecuados para la perfusión periférica. En el caso de un shock compensado, la perfusión será adecuada, pero a expensas de las demandas excesivas del corazón. Dependiendo del tipo y la gravedad de la insuficiencia cardiovascular y de la respuesta al tratamiento, el shock puede llegar a afectar a otros sistemas de órganos.
Hipovolemia
Como hemos comentado, en el quirófano, la causa más común de descompensación cardiovascular es la hipovolemia. 2
Ante pequeñas disminuciones de volemia, menos del 15%, el organismo utiliza sus mecanismos de compensación (aumento de la presión arterial y de la frecuencia cardíaca) para que el corazón continúe bombeando sangre y se disponga de los nutrientes adecuados. 4
Cuando se producen pérdidas más importantes, el organismo pierde su capacidad de compensación, o ésta no es suficiente, y el paciente entra en estado de shock.4
Las causas principales de shock hipovolémico son:
- Pérdida importante de sangre (shock hemorrágico).4
- Pérdida de agua y electrolitos (sodio y potasio).4
- Pérdida de plasma.4
Uno de los indicios de hipovolemia es la hipotensión, no obstante, otros signos evidentes de hipovolemia progresiva, así como la respuesta a su tratamiento, pueden ser difíciles de detectar sin la ayuda de un monitor avanzado que muestre los cambios hemodinámicos en tiempo real. 2
¿Cómo evitar la hipovolemia?
Cuando nos encontramos ante un paciente en shock hipovolémico, el objetivo es controlar la pérdida de líquido y sangre, reemplazar lo que se ha perdido y estabilizar el daño que causó y resultó del shock hipovolémico lo antes posible. 8
La reanimación con líquidos por vía intravenosa sigue siendo la intervención más común para los pacientes en situaciones críticas. Se ha debatido mucho sobre qué fluidos intravenosos utilizar para la reanimación, no obstante, actualmente las soluciones cristaloides siguen siendo el estándar de atención para la reanimación con líquidos.9

Te puede interesar:
Cristaloides y coloides en la reanimación del paciente crítico
Después de seleccionar el líquido intravenoso apropiado para la reposición, se debe fijar un objetivo terapéutico y monitorizar la evolución del paciente para poder controlar su respuesta y ajustar el tratamiento en base a esta.
Además, es muy importante contar con información en tiempo real ya que, en pacientes con hipovolemia grave o shock hipovolémico, el retraso en la fluidoterapia puede provocar una lesión isquémica y un shock irreversible desencadenando un fallo multiorgánico. 3
Por tanto, para poder identificar los primeros indicios de hipovolemia, y en caso de que esta se produzca, actuar precozmente, deberemos:
- Llevar a cabo una fluidoterapia guiada por objetivos.
- Contar con un sistema de monitorización que permita conocer tanto variables hemodinámicas clásicas como avanzadas a tiempo real, para poder identificar cualquier alteración en el estado del paciente y servir de guía durante la terapia.
Terapia guiada por objetivos
La terapia guiada por objetivos (GDT) permite un uso más adecuado de los fluidos, vasopresores e inotrópicos y, por tanto, ofrece un mejor pronóstico y una recuperación más rápida.
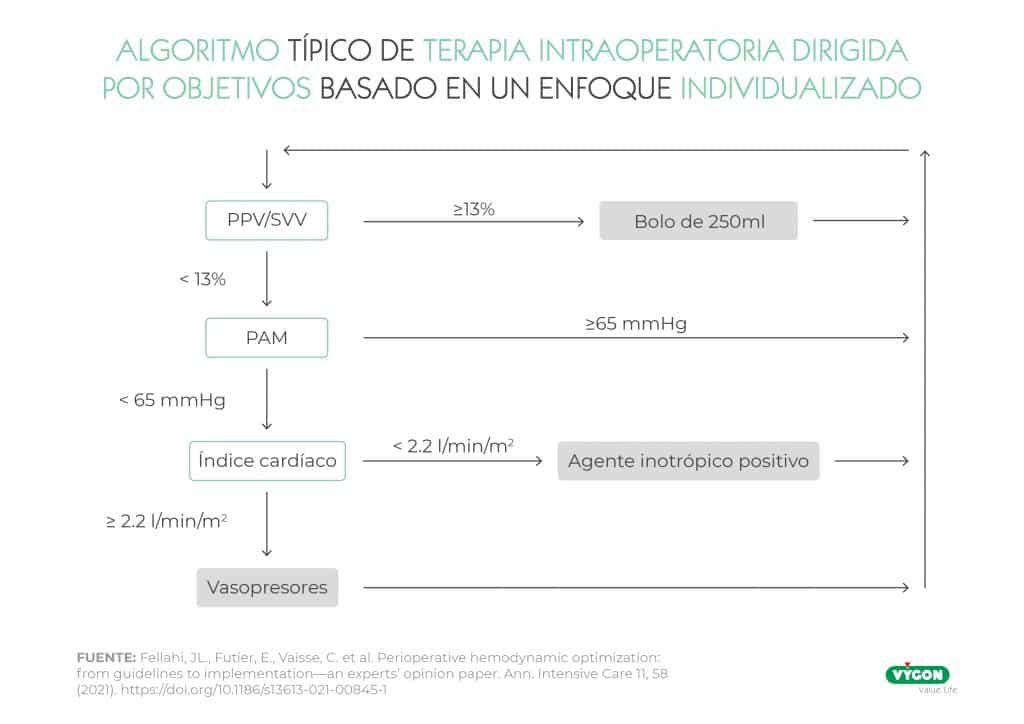
Se ha demostrado que la terapia perioperatoria dirigida por objetivos (PGDT) puede mejorar el resultado postoperatorio en pacientes de cirugía de alto riesgo.
Tal es la importancia de una fluidoterapia estricta, que la hipovolemia no corregida da lugar a infusiones inapropiadas de agentes vasopresores, lo que puede provocar un aumento de la hipoperfusión e isquemia de órganos. Por su parte, la reanimación con líquidos excesiva se ha asociado con un aumento de las complicaciones, una mayor duración de la estancia hospitalaria y en la unidad de cuidados intensivos (UCI) con un aumento de la mortalidad.
Te puede interesar:
Terapia guiada por objetivos. ¿cómo saber qué cantidad de líquidos administrar?
Monitorización en tiempo real
La monitorización hemodinámica determinará, en gran parte, la eficacia del tratamiento. Dentro de los sistemas avanzados de monitorización hemodinámica, los más empleados en pacientes de alto riesgo son aquellos que analizan el contorno del pulso de la onda de presión arterial (PCM) para la estimación del volumen sistólico.
Existen diferentes sistemas de monitorización disponibles, dos de los aspectos más importantes a la hora de elegir nuestro monitor es la invasividad y la precisión, que vendrá determinada por la forma que tiene de recoger la información el sistema.
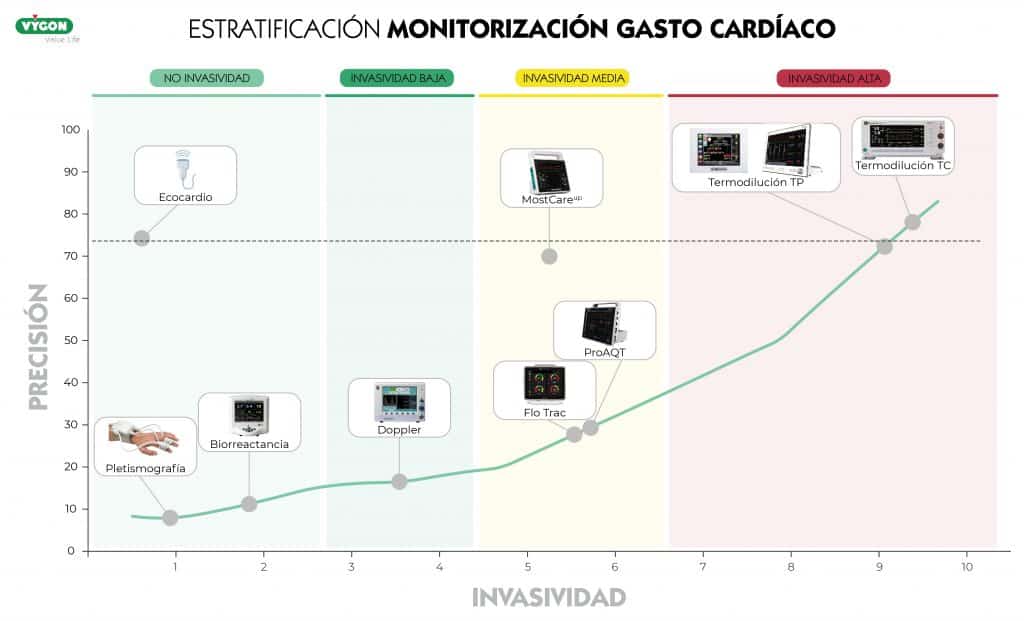
Por una parte, tenemos aquellos que utilizan las leyes de la física clásica (ley de Otto Frank y ley de Stewart Hamilton) los cuales son más precisos y, por otra, aquellos basados en métodos estadísticos (Langewouters, curtosis).
Estos últimos son menos invasivos, pero al partir de datos preestablecidos, sin contemplar las diferencias hemodinámicas individuales e independientes de la edad y el sexo, su precisión es baja.
Como hemos visto, ante pacientes que sufren o tienen probabilidades de sufrir hipovolemia, el factor tiempo tiene un papel fundamental, por ello, la sencillez o aparatosidad de conectar el sistema, la frecuencia de muestreo, la necesidad de calibración, o no, ante cada posible variación en los parámetros y la disponibilidad inmediata, latido a latido, de la información hemodinámica sonpuntos clave a tener en cuenta, ya que la respuesta del paciente puede ser impredecible y variar en breves instantes.
De forma general, los métodos físicos son más precisos que los métodos estadísticos, pero también son más invasivos, excepto el método P.R.A.M. que está considerado mínimamente invasivo.
Te puede interesar:
Riesgos de una monitorización hemodinámica altamente invasiva
La duración y magnitud de la hipovolemia determinarán:
- Daño renal agudo. 2
- Duración de la estancia. 2
- Mortalidad. 2
Cuanto más se tarde en detectar la hipovolemia, las complicaciones serán de mayor gravedad llegando a encontrarnos con graves complicaciones futuras o incluso la muerte.
Parámetros hemodinámicos
Para identificar y actuar desde los primeros indicios de la hipovolemia es importante contar con un sistema que muestre diferentes parámetros hemodinámicos clásicos y avanzados en tiempo real.
Cuando nos encontramos ante estados, o posibles estados, de hipovolemia, los parámetros hemodinámicos dinámicos serán más preciso s para determinar su etiología y la respuesta del paciente a la reposición de líquidos. 9
Variación de la presión del pulso (PPV) y la variación del volumen sistólico (SVV)
En estos pacientes, además de los parámetros clásicos de gasto cardíaco (GC), volumen sistólico (VS) o parámetros de presión, también son muy útiles la variación de la presión del pulso (PPV) y la variación del volumen sistólico (SVV). Se trata de dos parámetros muy relevantes para predecir respuesta del paciente a la infusión de volumen, aunque no todos los monitores cuentan con ellos. En caso de no disponer de estas variables, utilizando los cambios en la precarga y la presión de la aurícula derecha, la presión arterial, la presión del pulso o el volumen sistólico es posible calcularlos, no obstante, eso retrasaría nuestra actuación con el riesgo que esto conlleva. 9
Tanto la PPV como la VVS están consideradas como predictores fiables para medir la respuesta del GC a la infusión de fluidos, por lo que nos permitirán seguir de cerca la evolución del tratamiento administrado.
Elastancia dinámica (PPV/VVS)
Por otra parte, encontramos la elastancia dinámica (PPV/VVS) que es el cociente entre la variación de la presión del pulso (PPV) y la variación del volumen sistólico (SVV) durante una sola respiración con presión positiva. Este parámetro nos permitirá evaluar el tono arterial dinámico.
Elastancia arterial (Ea)
Otro parámetro dinámico interesante en la evaluación y prevención de la hipovolemia es la elastancia arterial (Ea), es decir, el cociente entre los cambios de presión telesistólica y los cambios de volumen sistólico, analizados desde un punto de vista dinámico. Este parámetro está principalmente relacionado con la elasticidad del sistema arterial.
La elasticidad de las grandes arterias permite que estos vasos se expandan durante la fase de eyección, alojando más sangre, y así asegurar el flujo sanguíneo diastólico en la periferia durante la diástole. Dado que el flujo arterial es cíclico, no constante, este parámetro ofrece información adicional de la postcarga dinámica (pulsátil) junto con la información de la postcarga estática (laminar) derivada de las Resistencias Vasculares Sistémicas (RVS).
Cuanto más rígidos son los vasos, menor es el volumen, y por tanto mayor es el Ea. Es decir, aporta información sobre cuál es la carga elástica impuesta al ventrículo izquierdo en cada latido.
Eficiencia del ciclo cardíaco (CCE)
Por último, la eficiencia del ciclo cardíaco (CCE) también resultaría útil ya que aporta información sobre la cantidad de energía que está gastando el sistema cardiovascular en eyectar la sangre en cada sístole.
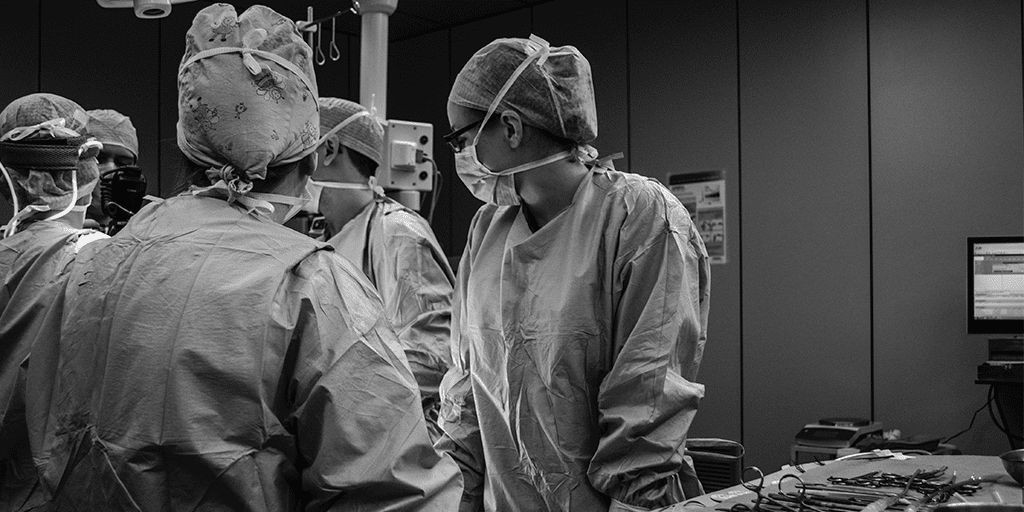
Entonces… ¿cómo de importante es el factor tiempo en pacientes que pueden sufrir hipovolemia?
Como hemos estado viendo, en los pacientes con hipovolemia, un retraso en la administración de líquidos puede provocar:
- Hipovolemia grave o shock hipovolémico.
- Lesión isquémica.
- Shock irreversible con fallo del sistema multiorgánico.
- Mayor duración de la estancia en la unidad de cuidados intensivos (UCI) y en el hospital
- Muerte.
Contar con un monitor sencillo de conectar, sin necesidad de calibraciones continuas y capaz de mostrar parámetros hemodinámicos clásicos y avanzados, en tiempo real, proporciona al profesional de la agilidad e inmediatez necesaria para tener una respuesta más rápida y evitar que el paciente evolucione de forma desfavorable.

Para conocer más sobre monitorización hemodinámica con el método P.R.A.M., matricúlate en el curso impartido por el Dr. José Miguel Alonso Iñigo, médico especialista en Anestesiología-Reanimación y Tratamiento del dolor. Para ello, solo tienes que hacer clic aquí o en el siguiente banner.
El método P.R.A.M. presenta una alta precisión y una invasividad media, lo que permite disponer de información exacta del estado hemodinámico del paciente disminuyendo riesgos relacionados con sistemas más cruentos.

Delegada especialista en Cuidados Intensivos.
- EXPERIENCIA
Farmacéutica de formación en la mención Clínica y Asistencial, con un Máster en Industria Farmacéutica, tengo tanto experiencia en Oficina de Farmacia, concretamente 7 años, como en la Industria Farmacéutica, 6 años hasta la fecha.
- PUEDO AYUDARTE EN…
Como especialista en cuidados intensivos, puedo ayudarte a darle un cuidado integral, óptimo y de calidad a tus pacientes críticos, sin perder de vista la humanidad que hay en ello. Además, me apasionan la seguridad de paciente y la prevención de las infecciones.
Delegado de ventas – Granada, Almería y Jaén
BIBLIOGRAFÍA
- Aseni, P., Orsenigo, S., Storti, E. et al. Current concepts of perioperative monitoring in high-risk surgical patients: a review. Patient Saf Surg 13, 32 (2019). https://doi.org/10.1186/s13037-019-0213-5
- Pinsky, M. R., Wertz, A., Clermont, G., & Dubrawski, A. (2020). Parsimony of Hemodynamic Monitoring Data Sufficient for the Detection of Hemorrhage. Anesthesia and analgesia, 130(5), 1176–1187. https://doi.org/10.1213/ANE.0000000000004564
- Mandel, J., Palevsky, P.M., (2021) Treatment of severe hypovolemia or hypovolemic shock in adults. Ed. Sterms, R.H., Manaker, S., Finlay, G. https://www.uptodate.com/contents/treatment-of-severe-hypovolemia-or-hypovolemic-shock-in-adults
- Ormaechea Alegre, E. Shock hipovolémico, causas y tratamiento. Salud Mapfre. https://www.salud.mapfre.es/enfermedades/cardiovasculares/shock-hipovolemico/
- Moranville MP, Mieure KD, Santayana EM. Evaluation and Management of Shock States: Hypovolemic, Distributive, and Cardiogenic Shock. Journal of Pharmacy Practice. 2011;24(1):44-60. doi:10.1177/0897190010388150
- Jacob L. Heller, MD, MHA, Emergency Medicine, Emeritus, Virginia Mason Medical Center, Seattle, WA. Also reviewed by David Zieve, MD, MHA, Medical Director, Brenda Conaway, Editorial Director, and the A.D.A.M. (2019). Shock. https://medlineplus.gov/spanish/ency/article/000039.htm
- Marik, P.E., Monnet, X. & Teboul, JL. Hemodynamic parameters to guide fluid therapy. Ann. Intensive Care 1, 1 (2011). https://doi.org/10.1186/2110-5820-1-1
- Nall, R. M. (2018, 17 septiembre). Hypovolemic Shock. Healthline. https://www.healthline.com/health/hypovolemic-shock
- Melendez Rivera JG, Anjum F. Hypovolemia. [Updated 2021 Jul 6]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2021 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK565845/
- Urbano J, López J, González R, Fernández SN, Solana MJ, Toledo B, Carrillo Á, López-Herce J. Comparison between pressure-recording analytical method (PRAM) and femoral arterial thermodilution method (FATD) cardiac output monitoring in an infant animal model of cardiac arrest. Intensive Care Med Exp. 2016 Dec;4(1):13. doi: 10.1186/s40635-016-0087-0. Epub 2016 Jun 3. PMID: 27256288; PMCID: PMC4891310.
- Gil Cano, A., Monge García, M., & Baigorri González, F. (2012). Evidencia de la utilidad de la monitorización hemodinámica en el paciente crítico. Medicina Intensiva, 650–655. https://doi.org/10.1016/j.medin.2012.06.004
- Mateu Campos, M., Ferrándiz Sellés, A., Gruartmoner De Vera, G., Mesquida Febrer, J., Sabatier Cloarec, C., Poveda Hernández, Y., & García Nogales, X. (2012b). Técnicas disponibles de monitorización hemodinámica. Ventajas y limitaciones. Medicina Intensiva. Published. https://doi.org/10.1016/j.medin.2012.05.003
- Teboul JL, Saugel B, Cecconi M, De Backer D, Hofer CK, Monnet X, Perel A, Pinsky MR, Reuter DA, Rhodes A, Squara P, Vincent JL, Scheeren TW. Less invasive hemodynamic monitoring in critically ill patients. Intensive Care Med. 2016 Sep;42(9):1350-9. doi: 10.1007/s00134-016-4375-7. Epub 2016 May 7. PMID: 27155605.
- Alonso-Iñigo JM, Escribá FJ, Carrasco JI, Fas MJ, Argente P, Galvis JM, Llopis JE. Measuring cardiac output in children undergoing cardiac catheterization: comparison between the Fick method and PRAM (pressure recording analytical method). Paediatr Anaesth. 2016 Nov;26(11):1097-1105. doi: 10.1111/pan.12997. Epub 2016 Aug 27. PMID: 27565740.
- Scolletta S, Romano SM, Biagioli B, Capannini G, Giomarelli P. Pressure recording analytical method (PRAM) for measurement of cardiac output during various haemodynamic states. Br J Anaesth. 2005 Aug;95(2):159-65. doi: 10.1093/bja/aei154. Epub 2005 May 13. PMID: 15894561.
- Scolletta, S., Romano, S. M., & Giomarelli, P. (2006). Minimally Invasive Hemodynamic Monitoring Using the Pressure Recording Analytical Method. Yearbook of Intensive Care and Emergency Medicine, 192–202. https://doi.org/10.1007/3-540-33396-7_19
- Sorbara, C., Romagnoli, S., Rossi, A., & Romano, S.M. (2007). Circulatory Failure: Bedside Functional Hemodynamic Monitoring.






0 comentarios
Trackbacks/Pingbacks