El origen de las terapias intravenosas
Uno de los mayores avances tecnológicos ligados a la medicina es el de las terapias intravenosas.
A la cabeza de estas terapias, están las bombas de infusión; dispositivos que liberan cantidades determinadas de alimento, sangre o medicamentos directamente en el sistema circulatorio del paciente, bajo la piel o en el sistema nervioso central, como en el caso de la anestesia epidural.
Aunque los primeros intentos de terapia intravenosa de los que se tiene constancia datan del S XV, no fue hasta el S XVII que se inventó el primer dispositivo de acceso intravenoso que llevó a lograr con éxito la primera transfusión sanguínea en 1665.

A principios del S XIX se inventaron los primeros prototipos de bombas de infusión con la intención de controlar la tasa de flujo durante los procedimientos intravenosos.
Durante el siglo XX se afinaron las agujas, los tubos de goma se substituyeron por otros de plástico y se diseñaron bombas de vacío que reducían el riesgo de embolia gaseosa.
Pero no es hasta los años 70 cuando se inventa la primera bomba ambulatoria que permitía que los pacientes disfrutaran de libertad de movimiento, así como tratamientos extrahospitalarios para aquellos que requerían dosis precisas a intervalos regulares.
Las bombas elastoméricas

Las bombas elastoméricas son dispositivos médicos no electrónicos de un solo uso que infunden medicamento de forma controlada y a una velocidad específica. Son totalmente portátiles y fáciles de transportar por el paciente para tratamiento domiciliario.
Están formadas por una carcasa de plástico rígido que contiene un elastómero que libera una energía que se traduce, a su vez, en una presión constante sobre el fármaco a infundir. Su velocidad de flujo es controlada por un capilar calibrado presente en el tubo de infusión.
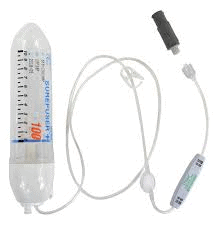
Aunque se emplean para diversos tratamientos y en varios servicios (infusión de antibióticos, retrovirales, unidades para el dolor crónico, etc), uno de los más extendidos es el su empleo en tratamientos de quimioterapia.
Peligro de la exposición laboral a fármacos antineoplásicos
Su empleo, cada vez más amplio, para los tratamientos de quimioterapia hace que tengan que utilizarse con medicamentos peligrosos (por ejemplo 5-fluaracilo), lo que supone un riesgo de exposición para los trabajadores, pacientes y cuidadores en la carga, manipulación, administración y retirada de este tipo de dispositivos.
En el año 2004, el National Institute for Occupational Safety and Health (NIOSH) de Estados Unidos en su publicación “NIOSH Alert: preventing occupational exposure to antineoplastic and other hazardous drugs in health care settings(1)” definió qué son los fármacos peligrosos y estableció 3 grupos, incluyendo en el grupo 1 a los fármacos antineoplásicos, debido a sus propiedades cancerígenas y/o mutágenas y/o tóxicas para la reproducción.
No obstante, ya desde el año 1979 tenemos evidencia de la relación entre la exposición laboral a fármacos antineoplásicos y los riesgos para la salud (Falck et al.)(2).
En dicho estudio, se analizó (mediante el test de Ames) el efecto mutágeno de los fármacos antineoplásicos a través de la orina de enfermeras que preparaban y administraban dichos fármacos sin medidas de protección.
Estudios posteriores han confirmado la posibilidad de daños para aquellos trabajadores expuestos a fármacos antineoplásicos, afectando a la gestación (3,4,5,6,7,8) (abortos, malformaciones), efectos crónicos (9,10) y efectos agudos (11,12).
Por tanto, se debe evitar de manera taxativa la exposición del personal sanitario y de los cuidadores a fármacos antineoplásicos.
¿Qué dice la ley?
En España, desde el 10 de febrero de 1996, está en vigor la Ley 31/1995, de 8 de noviembre, de Prevención de Riesgos Laborales. Esta Ley traspone la Directiva Europea 89/391/CEE, relativa a la aplicación de las medidas para promover la mejora de la seguridad y de la salud de los trabajadores, y tiene por objeto promover la seguridad y la salud mediante la aplicación de medidas y el desarrollo de las actividades necesarias para la prevención de riesgos derivados del trabajo.

Existe, por tanto, un marco legal que obliga a todas las empresas a proteger a sus trabajadores frente a los riesgos laborales.
Los familiares de los pacientes podrían estar también expuestos. Esta exposición podría darse tanto en el centro sanitario donde se recibe el tratamiento, como en su propio domicilio, debido a las secreciones del propio paciente o como consecuencia de las manipulaciones que se realicen, por ejemplo, en un infusor elastomérico.
Ante la evidencia científica y la exigencia legal nos debe surgir la pregunta:
¿Cómo prevenir la exposición a medicamentos peligrosos administrados por bombas de infusión elastoméricas?
No hay que olvidar que la última barrera física y legal para las personas expuestas son los equipos de protección individual (EPI´s), tales como mascarillas, guantes, batas y gafas. Según la etapa de manipulación del fármaco en la que estemos deberemos utilizar unos EPI´s y/u otros.
Estas etapas son:
En relación con la preparación:
El punto crítico durante la preparación del infusor elastomérico es la conexión y desconexión de la jeringa con fármaco, ya que tanto la presión ejercida como la ausencia de un sistema cerrado suponen un riesgo de exposición. Por ello, se deben aplicar las siguientes medidas de prevención:
Área de preparación:
deberá estar aislada de otras con antesala de almacenamiento, exclusa de paso y presión positiva en el interior.
Cabinas de seguridad biológica (CSB):
deberán estar certificadas y contar con marcado CE. La norma que deben cumplir las CSB es la UNE-EN 12469. Esta norma clasifica a las CSB en tres clases: Clase I, II y III. De las 3 clases son aptas para la preparación los tipos II y III.
La ubicación óptima de una CSB tiene que guardar una serie de distancias respecto a puertas, salidas y tomas de aire, y otras CSB (si hay más de una en la sala de preparación). Las CSB han de ser sometidas a revisión anual o plazo de tiempo inferior.
Sistemas cerrados de transferencia de medicamentos (CSTD en inglés):
Un CSTD es un dispositivo médico que impide mecánicamente el paso de los contaminantes ambientales al interior (protección del paciente) y el escape de medicamento peligroso al exterior de éste (protección del usuario). Esta definición, popularizada por el NIOSH en el año 2004, no dispone de una Norma nacional o internacional como si ocurre con las Cabinas de Seguridad Biológica (UNE-EN 12469). Por tanto, en la actualidad no está establecido un ensayo estandarizado que deban cumplir los CSTD para garantizar la protección, por lo que se debe solicitar al fabricante pruebas que garanticen el cumplimiento de la definición establecida por la NIOSH. La propia NIOSH está tratando de elaborar una norma propia para ensayar los CSTD y verificar que cumplen con su función de confinar al medicamento peligroso (13).
El trabajo con sistemas no cerrados dentro de las CSB provoca la contaminación de superficies de trabajo y de guantes (14,15). Esto nos demuestra que sería posible que los sistemas de infusión viniesen contaminados externamente por los propios fármacos antineoplásicos, con el riesgo que ello conlleva.
En relación con el transporte:
Deberá realizarse de forma que se eviten roturas o derrames en la forma de administración del fármaco, para lo que se emplearán sistemas y contenedores resistentes a golpes, específicos para estos medicamentos y con posibilidad de contener un posible derrame si éste se produjera.
En relación con la administración:
Los puntos críticos durante la administración del infusor elastómerico serán en la conexión a la vía de acceso al paciente, donde deberemos comprobar que la línea está purgada (eficacia del clampaje frente a la presión del infusor), y en la desconexión de la vía después de finalizada la infusión, donde la línea está con fármaco. Hay que considerar también la posibilidad de desconexiones accidentales o voluntarias.
En ambas situaciones es primordial el empleo de sistemas cerrados, pero sobre todo en la desconexión, ya que es la única medida para evitar la exposición a medicamentos peligrosos, a diferencia de la preparación que cuenta con un conjunto de medidas de prevención que explicamos anteriormente.
En relación con el desecho:
Una vez retirado el infusor elastomérico deberemos depositarlo en un contenedor específico para fármacos antineoplásicos (facilitado por la institución sanitaria si se hace en el domicilio o centro de salud) junto con los EPI´s utilizados en el proceso, y cerrarlo para su retirada.
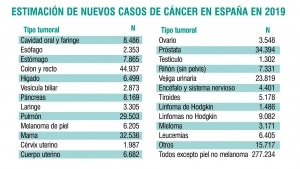
Debemos considerar que el número de tratamientos oncológicos aumenta cada año. Según la Sociedad Española de Oncología Médica, los nuevos casos han aumentado un 12% en los últimos 5 años (foto 1). Sin el empleo de las medidas correctas para la protección de la salud de trabajadores y familiares estamos agrandando el problema. Por ello es tan importante la información y formación que tengamos sobre los riesgos para la salud asociados al uso de infusores elastómericos empleados en Oncología.

Dr. Pablo Martín Lancharro
Salud Laboral y PRL (SERGAS)
Asesor de la SEEO (Sociedad Española en Enfermería Oncologica) en PRL.
Francisco J Menéndez González
CSTD Oncology Specialist
fmenendez@vygon.es
[accordion title=’Bibliografía’]
BIBLIOGRAFIA
1. NIOSH alert: preventing occupational exposure to antineoplastic and other hazardous drugs in health care settings. U.S. Department of Health and Human Services, Public Health Service, Centers for Disease Control and Prevention, National Institute for Occupational Safety and Health, DHHS (NIOSH) Publication No. 2004-165. [Consultado: 06/03/2018]. Disponible en: http://www.cdc.gov/niosh/docs/2004-165/pdfs/2004-165.pdf 2. Falck, K., Grohn, P., Sorsa, M., Vainio, H., Heinonen, E., Holsti, L.R., 1979. Mutagenicity in urine of nurses handling cytostatic drugs. Lancet. 1979 Jun 9;1(8128):1250-1. 3. Dranitsaris G, Johnston M, Poirier S, Schueller T, Milliken D, Green E and Zanke B. Are health care providers who work with cancer drugs at an increased risk for toxic events? A systematic review and meta-analysis of the literature. J Oncol Pharm practice. 2005; 11:69-78. 4. Bouyer J, Saurel-Cubizolles M-J, Grenier C, Aussel L and Job-Spira N. Ectopic pregancy and occupational exposure of hospital personnel. Scand J Work Environ Health. 1998; 24:98-103. 5. Hoffman DM. Reproductive risks associated with exposure to antineoplastic agents: a review of the literature. Hosp Pharm.1986; 21: 930-932. 6. McDonald AD, McDonald JC, Armstrong B, Cherry NM, Côté R, Lavoie J, Nolin AD and Robert D. Congenital defects and work in pregnancy. Br J Ind Med. 1988;45:581-588. 7. Peelen S, Roeleveld N, Heederik D, Krombout H and de Kort W. Toxic effects on reproduction in hospital personnel. 1999; Dutch Ministry of Social Affairs and Employment.. 8. Valanis B, Vollmer W, Labuhn K and Glass A. Occupational exposure to antineoplastic agents and self-reported infertility among nurses and pharmacists. J Occup Environ Med. 1997; 39:574-580. 9. Lassila O, Toivanen A and Nordman E. Immune function in nurses handling cytostatic drugs. Lancet. 1980; 2:482. 10.. Sessink PJM, Verplanke AJW, Herber RFM and Bos RP. Occupational exposure to antineoplastic agents and parameters for renal dysfunction. Int Arch Occup Environ Health. 1997; 69:215-218. 11. McDiarmid M and Egan T. Acute occupational exposure to antineoplastic agents. J Occup Med. 1988; 30:984-987. 12. Valanis BG, Vollmer WM, Labuhn KT and Glass AG. Acute symptoms associated with antineoplastic drug handling among nurses. Cancer Nurs. 1993; 16:288-295. 13. Cdc.gov. (2018). CDC – NIOSH Docket: A Performance Test Protocol for Closed System Transfer Devices Used During Pharmacy Compounding and Administration of Hazardous Drugs. [Internet]. [Consultado: 06/03/2018]. Disponible en: https://www.cdc.gov/niosh/docket/review/docket288a/default.html 14. Crauste-Manciet, S., Sessink, P., Ferrari, S, Jomier, J. and Brossard, D. Environmental Contamination with Cytotoxic Drugs in Healthcare Using Positive Aire Pressure Isolators. Ann. occup. Hyg. 2005; 49 (7): 619-628. 15. Ziegler, E., Mason, H.J. and Baxter, P.J. Occupational exposure to cytotoxic drugs in two UK oncology wards. Occup. Environ. Med. 2002; 59: 608-612Francisco J Menéndez González[/accordion]
¿Te interesa este tema?
Si quieres saber más acerca del manejo de fármacos antineoplásicos, rellena el formulario con tus datos y dudas e intentaremos ayudarte a resolverlas.
Tranquil@, esto NO es una lista de SPAM.
SOLO utilizaremos tus datos para responder a las preguntas que nos hagas.






0 comentarios
Trackbacks/Pingbacks