El 27 de noviembre de 1921 en el teatro Rialto de New Haven todo estaba preparado para exhibir “The Sheik”. El público estaba expectante, la venta de entradas había superado las expectativas, nadie podía imaginarse lo que sucedería esa noche.

Poco antes de comenzar la película un descuido hizo que el incienso que encendieron en el escenario, y que prometía crear una atmosfera perfecta para la visualización del filme, prendió las cortinas cercanas y pronto todo se convirtió en una nube de humo.
Esa noche cuatro personas perdieron la vida y al menos ochenta resultaron heridas, muchas de ellas de gravedad.
Frank Underhill fue el encargado de estudiar a las víctimas del incendio y descubrió que el líquido que rellena la ampolla y que se produce como respuesta a una lesión térmica, tiene una composición similar al plasma. A Underhill también le debemos la primera descripción precisa sobre la gravedad de la pérdida de líquido a través de las quemaduras.
Sus conceptos fueron la base del programa de reposición de volumen en quemados que llevaron a cabo Cope y Moore en Coconut Grove en 1942. Fue en este momento cuándo se introdujo la primera fórmula de reposición y se habló del término de edema por quemaduras.
Todos estos conceptos no han parado de perfeccionarse a lo largo de los años, con el objetivo principal de la reposición de volúmenes para recuperar y mantener la perfusión tisular, evitando de esta forma la isquemia orgánica y manteniendo los tejidos con daño reversible.
En segundo lugar, también se busca minimizar el edema que puede comprometer la función pulmonar o desencadenar la necrosis de tejidos afectados pero viables.
Para poder conseguir estos objetivos es necesario:
- Examinar al paciente: tamaño y profundidad de la quemadura.
- Elección de la ruta óptima para la reanimación.
- Conocer las diferentes fórmulas de reanimación en pacientes quemados.
- Dominar los cristaloides y coloides disponibles para el tratamiento.
Perfil del paciente quemado
El paciente gran quemado es, para muchos profesionales de la salud, un reto difícil al que enfrentarse por el gran número de complicaciones y por la alta mortalidad que presenta.
Tanto la atención inicial de los pacientes con quemaduras graves, como su manejo perioperatorio, presentan desafíos en el manejo de la vía aérea, el acceso vascular, la hemodinámica y en el soporte ventilatorio.
Además, los pacientes quemados precisan una mayor cantidad de líquidos en las primeras 24h. que cualquier otro paciente con trauma debido a los mecanismos fisiopatológicos que tienen lugar tras una quemadura.
Cuando la lesión térmica tiene una extensión superior al 20% de la superficie cutánea se produce una respuesta inflamatoria sistémica con síndrome de fuga capilar, apareciendo lo que conocemos como shock por quemadura. Una combinación de shock hipovolémico y shock celular, caracterizado por cambios microvasculares y hemodinámicos específicos.
Esta pérdida de plasma desde el espacio intravascular al espacio intersticial, tanto en el tejido sano como en el afectado, da lugar a edema, hipovolemia y hemoconcentración.
La inhalación de humo también jugará un papel importante en el tratamiento y pronóstico del paciente, ya que puede conducir a hipoxia tisular.
Estimación del tamaño y profundidad de la quemadura
El primer paso es analizar la extensión y profundidad de la quemadura. En algunos hospitales se llega a estimar hasta dos veces, debido a la alta complejidad e importancia de una correcta aproximación.
Actualmente existen herramientas de escaneo 3D que facilitan la tarea y permiten una mayor precisión en la estimación de las áreas quemadas.
Elección de la ruta óptima para la reanimación
Cuando las quemaduras superen el 20% de la superficie corporal del paciente la reposición de líquidos se realizará por vía intravenosa.
Las quemaduras, además, presentan una dificultad añadida en la elección del área donde poder insertar la vía venosa. La primera premisa será tratar de realizar la punción en un área no quemada.
Existe una escala de decisión para elegir la mejor alternativa dependiendo de cada paciente:
- Primera opción: vena periférica de grueso calibre en área no quemada.
- Segunda opción: vena central en área no quemada.
- Tercera opción: vena periférica de grueso calibre en área quemada.
- Última opción: siempre que no sea posible ninguna de las anteriores alternativas, se procederá a insertar la vía en la vena central aun siendo un área quemada.
La necesidad de reposición de líquidos en estos pacientes es muy alta y debe empezar cuanto antes. Con lo que disponer del material adecuado y que admita los flujos necesarios es esencial para evitar una resucitación tardía.
Aunque en un primer instante, en el lugar del accidente, la vía periférica será la más usada, una vez llegados a la Unidad de Quemados, la vía central será la que nos ofrezca mejores prestaciones para la atención integral al paciente quemado. Un catéter central con vía de alto flujo puede ser de gran utilidad, especialmente en las primeras horas/días.
¿Por qué utilizar catéteres de alto flujo?
De forma general, para un adulto de 70 kg y una superficie corporal quemada (SCQ) igual o superior al 20% la reanimación responderá a las siguientes metas:
- Líquidos de Reanimación (Fórmula Parkland)
4mlx70Kgx20%SCQ=5.600ml - Líquidos de Mantenimiento
100mlx10Kg=1.000ml
50mlx10Kg=500ml
20mlx50Kg=1.000ml
Total= 2.500ml
Por lo tanto, durante las primeras 24h un paciente de estas características precisará 8.100 ml de líquidos. Por ello siempre que se pueda se utilizará un catéter de alto flujo para la administración del tratamiento.
Inicio de la reanimación con fluidos
Una vez se haya examinado el área quemada y se haya seleccionado la vía más adecuada para llevar a cabo la reanimación, el clínico comenzará la fluidoterapia intravenosa. La cual, se realizará antes de las 2 horas desde la ocurrencia de la quemadura, para evitar el aumento del riesgo de morbilidad y mortalidad de los pacientes.
Con el fin de facilitar la administración de líquidos en el paciente quemado, desde 1942, tras el lamentable incendio en Boston en Cocoanut Grove Nightclub, no ha cesado la investigación sobre nuevas fórmulas que sirvan de guía para los profesionales ante esta difícil patología.
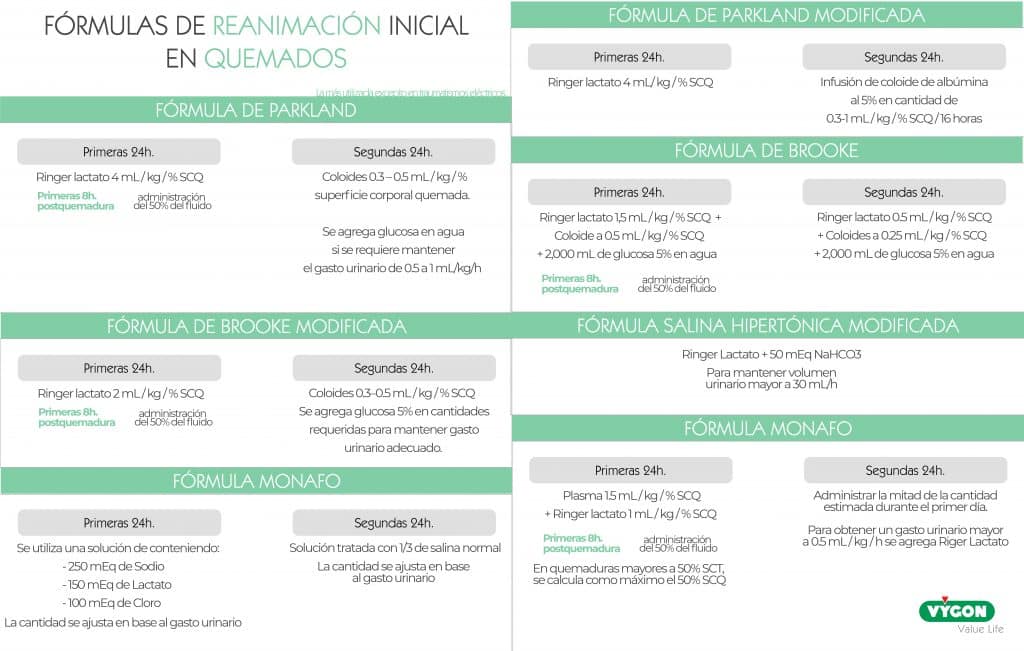
Las fórmulas para la reanimación del paciente quemado son:
- Parkland
- Parkland modificada
- Brooke
- Brooke modificada
- Monafo
- Salina hipertónica modificada
- Haifa
No obstante, estas fórmulas son únicamente un punto de partida. Cada paciente es diferente y el profesional será quién tome la decisión sobre la cantidad óptima que precisa el paciente.
La monitorización y una terapia dirigida por objetivos proporcionarán al clínico unos parámetros que le permitan tomar una decisión sobre la cantidad de coloides o cristaloides necesaria.
Reposición con cristaloides
Como comentábamos anteriormente, el líquido del edema en la quemadura es isotónico y su contenido protector tiene la misma proporción que el que se encuentra en el plasma. Por ello se produce la pérdida de plasma desde el espacio intravascular al espacio intersticial durante las primeras horas.
De esta premisa parte la fórmula más aplicada en la actualidad, la de Parkland. Que recomienda comenzar la reposición con cristaloides, en concreto con Ringer Lactato en una concentración de sodio de 130 mEq/t, durante las primeras 24 h.
Una vez pasado este tiempo y habiéndose recuperado la integridad capilar, se procederá a la administración de coloides.
Para calcular el requerimiento de cristaloides, la fórmula de Parkland recomienda la administración durante las primeras 24 horas de 4 mL/kg/% superficie corporal quemada (SCQ) de Ringer Lactato, administrando la mitad durante las primeras 8 h.
Todas las fórmulas que encontramos actualmente incluyen el Ringer Lactato durante las primeras 24 horas, aunque en diferentes proporciones. (tabla superior)
Soluciones cristaloides Hipertónicas
En 1970 W. Monafo propuso incluir las soluciones hipertónicas en cantidades de 240 a 300 mEq de Sodio, puesto que consideraba que producían menor edema.
Además del fluido hipertónico, de acuerdo con esta guía, durante las primeras 24 horas también se administrará 150 mEq de Lactato y 100 mEq de Cloro.
En las 24 horas posteriores la solución es tratada con 1/3 de salina normal. El indicador utilizado, en este caso, para conocer la respuesta a la reposición es la diuresis.
No obstante, algunos estudios han descrito que la infusión de fluido neto con soluciones hipertónicas es menor que con solución de Ringer Lactato. La diuresis es mayor y aumenta el edema intersticial, reflejado en un mayor flujo linfático. Esto se debe al desplazamiento de líquido desde el intracelular al extracelular como resultado de la solución hiperosmolar. [1] Lo cual da una apariencia externa de menor edema.
Reposición con coloides
Para mantener el volumen plasmático y evitar que se incremente el edema, las proteínas plasmáticas son especialmente necesarias, ya que la presión oncótica contrarresta a la presión hidrostática que provoca la fuga de líquido.
La fórmula de Evans, también conocida como fórmula de Brooke, tras su modificación por el Brooke Army Medical Center, propone el uso de coloides desde las primeras 24 horas.
Pero al igual que existe controversia respecto si la solución ideal debe ser isotónica o hipertónica, también existen diferentes posturas con respecto a la reposición con proteínas. Por lo que, formulas como Brooke modificada no aconsejan los coloides hasta pasadas las 24 horas.
Existen diversas fórmulas, todas buscan un mismo objetivo, reanimar al paciente quemado, pero cada una es diferente y propone distintas soluciones y cantidades para conseguirlo.
Por ello es tan importante la valoración clínica, las fórmulas deben utilizarse como herramientas para iniciar el tratamiento, pero será el clínico quién en función de la respuesta del paciente irá ajustándose a las necesidades individuales.
Esta cantidad deberá responder a la recuperación de las funciones orgánicas sin producir cambios patológicos iatrogénicos. Mientras la velocidad de administración se enfocará en asegurar una diuresis aproximada de 30 cc/hora en adultos.
Muchos han sido los avances e investigaciones desde que en 1921 Frank Underhill viviera la catástrofe del Teatro Rialto de New Haven. Nuevos dispositivos como equipos de monitorización hemodinámica o los catéteres de alto flujo le podrían haber ayudado a ajustar la terapia de sus pacientes y administrar el volumen necesario.
También las fórmulas habrían sido una gran herramienta para la reanimación de los heridos. Un excelente punto de partida para dirigir su terapia, ya que, hoy en día, si se aplican de manera correcta, presentan una tasa de fallo menor del 5% en pacientes con quemaduras de hasta 85% de superficie corporal. [2]
Los avances no cesan, todos los días hay profesionales que se preguntan cómo pueden optimizar la terapia y es gracias a ellos y sus investigaciones que cada día los porcentajes de recuperación son mejores.
Bibliografía
- Warden G. Burn shock resuscitation. World J Surg 1992: 16: 16-23.
- Iribarren B, Osvaldo y cols. Fisiopatología y reposición de volumen en el paciente quemado agudo. Revista chilena de cirugía. Volumen 48 Nº5 Octubre 1996.
- P. Guilabert, G. Usúa, N. Martín, L. Abarca, J. P. Barret, M. J. Colomina, Fluid resuscitation management in patients with burns: update, BJA: British Journal of Anaesthesia, Volume 117, Issue 3, September 2016, Pages 284–296
- Aguilera Castro, Fernando. Anestesia y manejo perioperatorio del paciente quemado. Revista Salud Bosque. Volumen 6, Número 1, Págs. 65-78
- Dra Gemma Usúa Lafuente. Anestesia en el paciente quemado. Curso sobre anestesia en especialidades quirúrgicas 2015-2016
- Rita Mª Galeiras Vázquez, Juan J. García Barreiro, Mª Eugenia López Suso. Asistencia inmediata al paciente quemado crítico. Complejo Hospitalario Universitario A Coruña. ISBN: 978-84-615-2921-6
- Dr. Jaime Vázquez-Torres, Dra. Ofelia Zárate-Vázquez. Manejo de líquidos en el paciente quemado. Anestesia en el paciente con trauma. Vol. 34. Supl. 1 Abril-Junio 2011
- M.Basora, M.J.Colominab, V.Moralc, M.S.AsuerodeLisd, E.Boixe, J.L.Joverf, J.V.Llaug, M.P.Rodrigoh, J.Ripollési y J.M.CalvoVecinoj. Guía de práctica clínica para la elección del fluido de restauración volémica perioperatoria en los pacientes adultos intervenidos de cirugía no cardiaca. Rev. Esp. Anestesiol. Reanim.2016;63(1):29-47
- Ministerio de salud. Guía Clínica. Manejo del paciente gran quemado. Santiago: Minsal, 2016





0 comentarios
Trackbacks/Pingbacks