¿Te has preguntado alguna vez si el catéter que estás utilizando en tu paciente neonatal es capaz de proporcionar el flujo que realmente tu necesitas?
En muchas ocasiones surgen dudas sobre si un catéter de pequeño calibre o un PICC neonatal de un solo lumen podrá mantener la infusión continua de una medicación esencial, de una nutrición parenteral completa a ritmo alto o la infusión simultánea de varias infusiones. En neonatología, especialmente en neonatos extremos, la elección del calibre, longitud y material del catéter es crucial para mantener infusiones seguras y eficaces. Este artículo aborda una estimación de los flujos máximos que permiten infundir los distintos tipos de catéteres de pequeño calibre utilizados habitualmente en el paciente neonatal, así como los principales factores que pueden modificar estos valores y cómo optimizar su uso clínico.
Las fichas técnicas de las diferentes casas comerciales ofrecen una orientación aproximada sobre los flujos máximos de sus catéteres en condiciones de laboratorio. Estas estimaciones se obtienen bajo presiones determinadas y controladas, en general puede encontrarse a caída libre, presiones de 1 bar (750 mmHg) o incluso a presiones máximas del propio catéter expresados en ml/min, pero no representan flujos óptimos ni seguros en el contexto clínico real. De hecho, aplicar esas cifras en la práctica puede poner en riesgo tanto la integridad del dispositivo como la seguridad del propio paciente. Someter el catéter a presiones superiores a 21,75 psi (1,5 bar, 1125mmHg) puede dar lugar a la rotura del catéter y embolia.
Por ello, en este artículo presentamos una tabla con flujos teóricos más realistas, calculados bajo condiciones que simulan de forma más fiel la práctica clínica. En concreto, si consideramos una presión de trabajo máxima de 100 mmHg, lo que representa un margen de seguridad aceptable y suficiente para garantizar una administración efectiva y segura sin generar sobrepresión que ponga el riesgo la integridad del dispositivo.
Estimación teórica de los flujos de infusión
Los flujos que se muestran se han calculado considerando soluciones bajo condiciones ideales de laboratorio, con presiones estándar de 1 bar (750 mmHg) y los flujos obtenidos hasta 100 mmHg de presión máxima, expresados en ml/h. Estas condiciones simulan un contexto más próximo a la realidad clínica y práctica para la toma de decisiones.
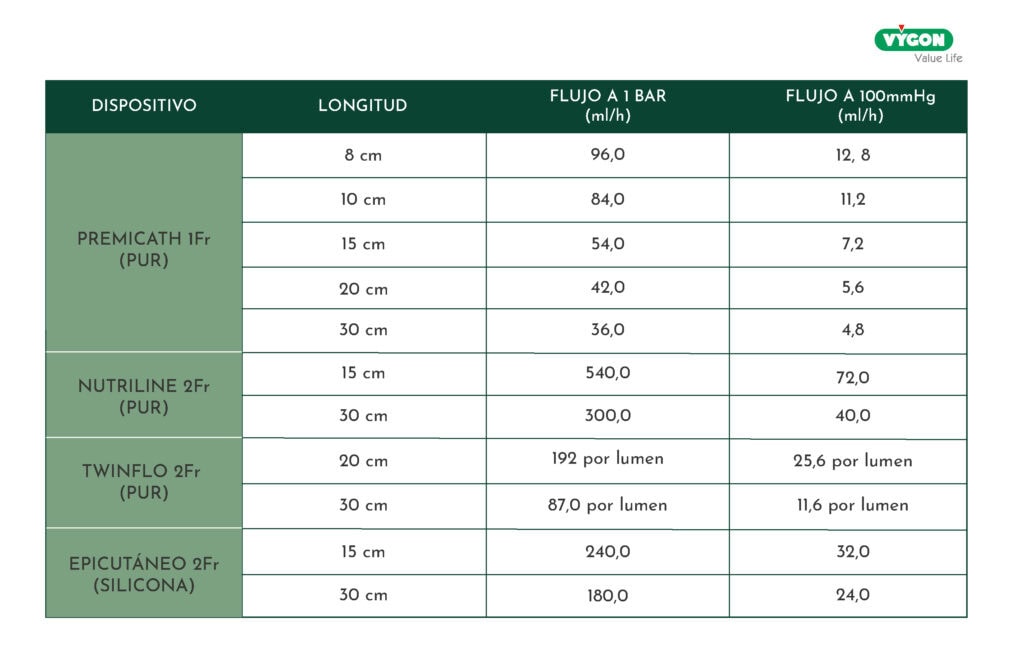
Factores que modifican el flujo efectivo
Aunque la presión aplicada es el factor principal que determina el flujo a través de un catéter, existen otros elementos clave que pueden afectar de forma importante:
1. Calibre, longitud y material del catéter
A mayor calibre, mayor flujo y en igualdad de calibres a mayor longitud, menor flujo. Además, el material del catéter también juega un papel determinante. Por ejemplo, los catéteres de silicona, aunque biocompatibles, requieren una pared más gruesa en su construcción, lo que reduce la luz interna. A igualdad de calibre y longitud, los catéteres de silicona pueden tolerar flujos significativamente menores que los de poliuretano.
2. Posición de la punta y disposición anatómica
Catéteres en posiciones anatómicas subóptimas —por ejemplo, dirigidos hacia la pared del vaso o ubicados en zonas de confluencia venosa con ángulos cerrados o acodamientos— pueden dificultar la progresión del flujo o generar aumentos de presión detectados por la bomba. En un 28% de los PICC migran en los primeros 24-72h, y un 40% antes de su retirada lo que puede incrementar los riesgos asociados.
Además, zonas de inserción como la fosa antecubital o el hueco poplíteo pueden favorecer la flexión del catéter, especialmente si se emplean dispositivos de poliuretano, que tienen una mayor memoria y, por tanto, menor capacidad de recuperación de su forma original frente a los de silicona. Esto puede traducirse en una limitación sostenida del flujo durante todo el tiempo de uso del dispositivo.
3. Altura relativa de la bomba de infusión
La altura a la que se encuentra la bomba respecto al paciente puede generar una presión positiva o negativa adicional percibida por la bomba:
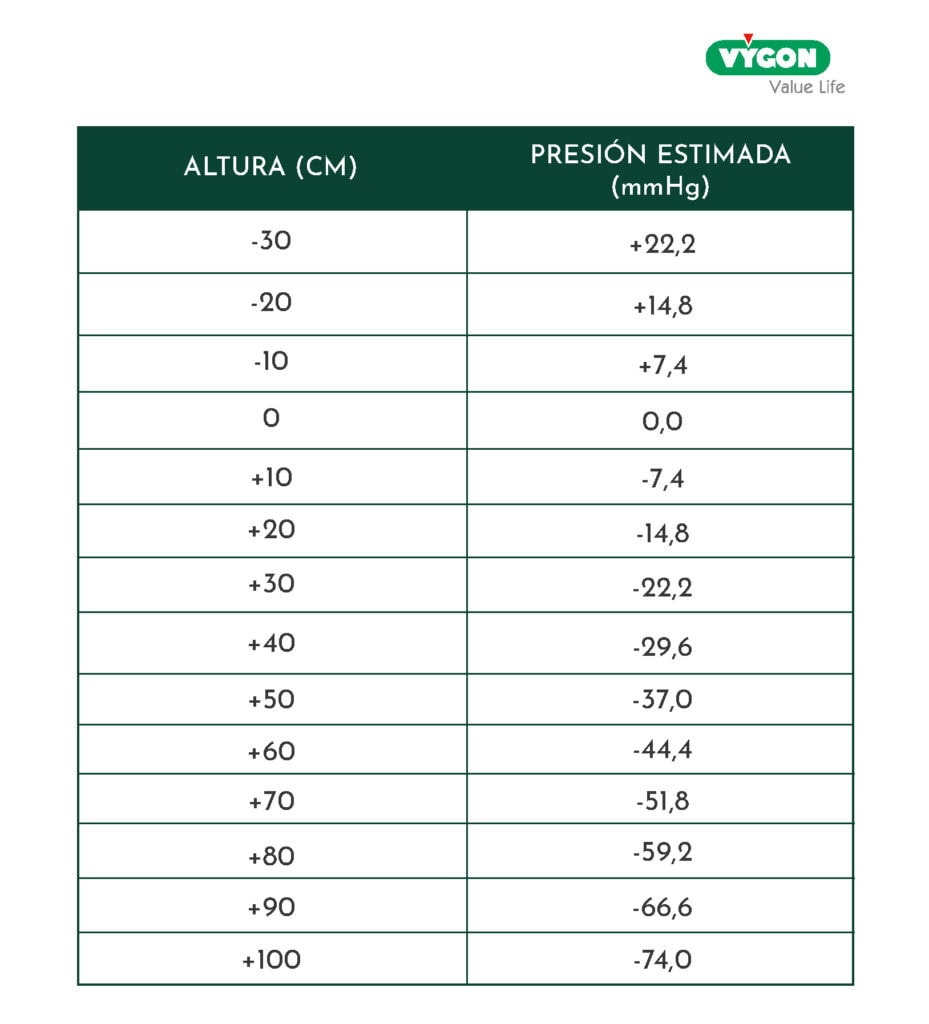
4. Resistencias y tipos de conexiónes
Unión luer-lock, válvulas antirreflujo, alargaderas y filtros de partículas pueden añadir resistencia adicional al sistema, disminuyendo el flujo efectivo. Esto puede pasar desapercibido, pero tener un impacto clínico real.
Importancia de la monitorización de la presión en la infusión
La monitorización continua de las presiones de infusión es un recurso clave para el manejo seguro de los catéteres vasculares en neonatología. Las bombas de infusión modernas permiten establecer límites máximos de presión para cada infusión, generalmente alrededor de 200 mmHg. Estos límites funcionan como barreras de seguridad: si durante la administración la presión alcanza el umbral prefijado, la bomba detiene temporalmente la infusión y emite una alarma que indica una posible oclusión o una resistencia anómala. A continuación, el dispositivo reduce el exceso de presión retrayendo el gatillo o el pistón del émbolo, lo que permite extraer el volumen que genera la sobredistensión del sistema y descontar dicho volumen, no administrado al paciente.
Este mecanismo protege tanto al paciente como al catéter, evitando la sobrepresión que podría derivar en extravasaciones, lesiones endoteliales o incluso en daños estructurales al dispositivo. Sin embargo, es fundamental comprender que cuando se activa una alarma de oclusión, habitualmente la infusión no está llegando al paciente. Esto convierte a la presión de infusión en un indicador indirecto del estado del sistema, pero también en un parámetro clínicamente relevante: una infusión considerada crítica no debería permanecer sin administrarse durante un periodo prolongado sin intervención. Por tanto, es prioritario no solo ajustar los límites de presión según la situación clínica y el tipo de catéter, sino también realizar una vigilancia activa de las fluctuaciones de presión como signo temprano de posibles complicaciones o de la interrupción en la administración de dicha infusión.
MANTENIMIENTO DEL CATÉTER
Además, cuando se utilizan catéteres para múltiples infusiones o para la administración secuencial de diferentes fármacos, es crucial realizar lavados adecuados entre medicaciones. Las recomendaciones actuales para prevenir y minimizar los riesgos de daños en el catéter están basadas en el uso de jeringas con émbolo de 10 mililitros. Sin embargo, en aquellas situaciones en las que se administran pequeñas cantidades en bolo—incluso inferiores a 1 ml, administradas con jeringas de 1 ml— se recomienda aplicar el bolo de forma lenta, en aproximadamente un minuto, para reducir la presión generada dentro del catéter y minimizar los riesgos de daños estructurales.
Tras la infusión de medicamentos o soluciones incompatibles, se recomienda lavar el catéter con un volumen de suero fisiológico equivalente a 2 o 3 veces el espacio muerto del sistema completo, incluyendo el propio catéter, las alargaderas y las válvulas, con el fin de prevenir precipitados o interacciones peligrosas.
CONCLUSIONES
La optimización del flujo de infusión en catéteres PICC en neonatos es un aspecto crucial para garantizar tanto la eficacia terapéutica como la seguridad del paciente. Conocer los límites reales de estos dispositivos, más allá de los valores teóricos proporcionados por los fabricantes, permite tomar decisiones clínicas más ajustadas a la práctica asistencial. Factores como el calibre y la longitud del catéter, su composición, la anatomía del trayecto venoso, la altura de la bomba de infusión y el tipo de conexiones empleadas pueden modificar de forma significativa el flujo efectivo y la presión interna del sistema. Por tanto, deben ser cuidadosamente considerados al seleccionar el catéter más adecuado en casos clínicos complejos.
Además, una adecuada monitorización de la presión de infusión, el uso correcto de jeringas y la aplicación sistemática de lavados con volúmenes suficientes tras la administración de fármacos son medidas clave para prevenir complicaciones y preservar la integridad del acceso vascular.
A pesar de los avances técnicos, aún existen áreas que requieren mayor investigación: la validación clínica de los flujos estimados a distintas presiones, el análisis del impacto de nuevos materiales sobre la dinámica de infusión en neonatos extremos, o el desarrollo de algoritmos predictivos de oclusión precoz. Integrar estos conocimientos con herramientas de monitorización inteligente podría abrir la puerta a una gestión más precisa y segura de los catéteres PICC en el paciente neonatal.
RESUMEN
- Elige el catéter con criterio: 1 Fr suele soportar <7–10 ml/h a ≤100 mmHg; 2 Fr permite mayores flujos pero deben poder ajustar ratio ocupación del vaso del 33-45%.
- Controla la posición de la punta: hasta un 41 % migran antes de ser retiro; las migraciones aumentan el riesgo de extravasación.
- Monitorea la presión de infusión: establece límites según el tipo de catéter y terapia.
- Reduce resistencias externas: minimiza accesorios que puedan disminuir el flujo.
- Realiza lavados adecuados: 2–3 volúmenes del espacio muerto y bolos lentos son fundamentales.
BIBLIOGRAFÍA
- Chopra V, Flanders SA, Saint S, et al. The Michigan Appropriateness Guide for Intravenous Catheters (MAGIC). Ann Intern Med. 2015;163(6 Suppl):S1-S40.
- Raad II, Darouiche RO, Dupuis J, et al. Central venous catheters coated with minocycline and rifampin for the prevention of catheter-related colonization and bloodstream infections: a randomized, double-blind trial. Clin Infect Dis. 1997;25(5):1116-1121.
- Gorski LA, Hadaway L, Hagle ME, et al. Infusion Therapy Standards of Practice. J Infus Nurs. 2021;44(1S Suppl 1):S1-S224.
- Pichler J, et al. Flushing and Locking of Venous Catheters: A Review of the Literature. J Hosp Infect. 2020;104(2):97-104.
- ECRI Guidelines Trust. Guidelines on infusion therapy safety. 2024.





0 comentarios