Tra i diversi rischi associati all’assistenza sanitaria e socio-sanitaria, quello infettivo, ossia il rischio per pazienti e operatori di contrarre un’infezione nel corso di un episodio assistenziale o in ambito lavorativo, occupa un posto particolare in ragione delle dimensioni del rischio.
Infatti, in media, il 5% dei pazienti ospedalizzati contrae un’infezione durante il ricovero (ICA).
Non tutte le ICA sono prevenibili, perché in alcuni casi l’infezione è solo temporalmente associata all’episodio assistenziale, senza essere imputabile ad alcun fattore modificabile: i microrganismi fanno parte della flora endogena del paziente e l’insorgenza dell’infezione è attribuibile alle sue particolari condizioni cliniche. Studi recenti hanno però dimostrato come la quota prevenibile sia molto più ampia di quanto creduto fino a poco tempo fa.
Ogni anno, quindi, si verificano in Italia tra le 450mila e le 700mila infezioni in pazienti ricoverati in ospedale (soprattutto infezioni urinarie, seguite da infezioni della ferita chirurgica, polmoniti e sepsi).
Le sepsi corrispondo a circa il 5% delle infezioni nosocomiali e tra queste devono essere annoverate le infezioni ematiche catetere-correlate (CRBSI) che sono frequenti, costose e potenzialmente letali.
Catheter-Related Bloodstream Infection (CRBSI)
Per CRBSI si intende una batteriemia che si verifica almeno 48 ore dopo il posizionamento di un CVC senza apparenti infezioni di altri siti e, in genere, si possono prevenire grazie ad un’accurata gestione del sito di emergenza del catetere e della linea infusionale.
Esse sono causate da batteri che arrivano nel circolo ematico dall’esterno per via intra o extra-luminale o da altri foci infettivi già presenti nell’organismo ospitante.
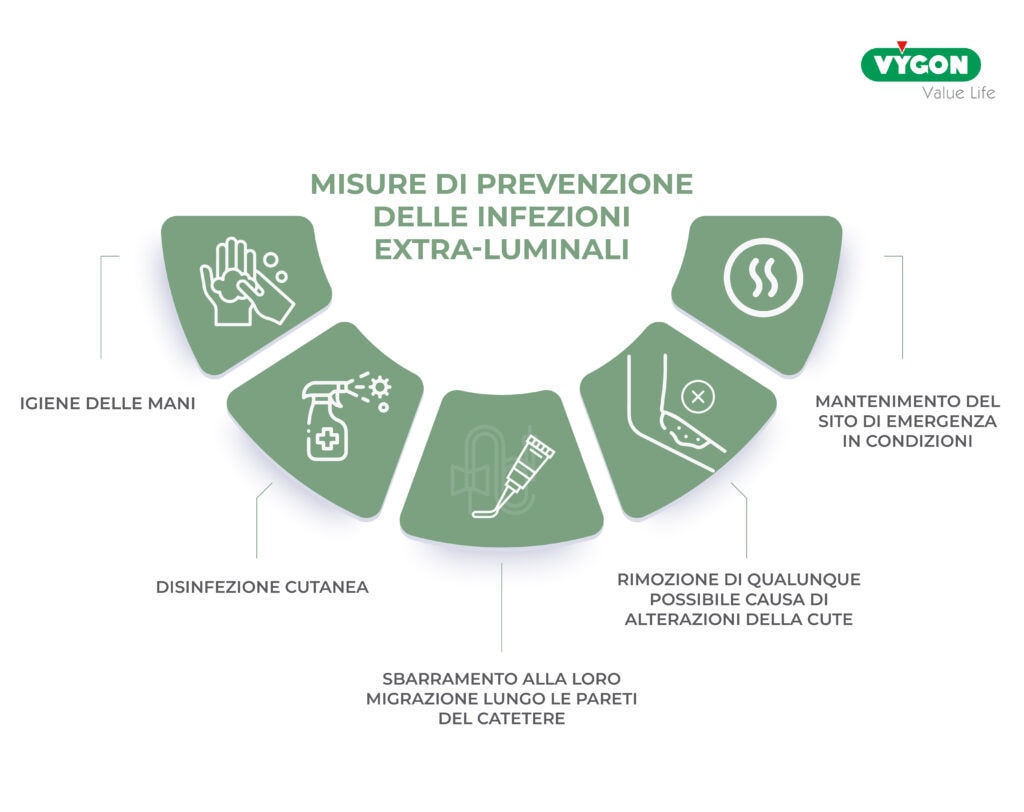
Le infezioni extra-luminali sono causate da batteri che migrano verso il circolo sanguigno lungo le pareti esterne del catetere.
Si tratta dei batteri che colonizzano la cute circostante il sito di emergenza del catetere che possono essere contrastati con diverse misure.
Le infezioni intra-luminali sono causate da batteri che migrano verso il circolo sanguigno passando all’interno del lume del catetere ed in genere si innescano nel momento in cui si accede alla porta di infusione del catetere.

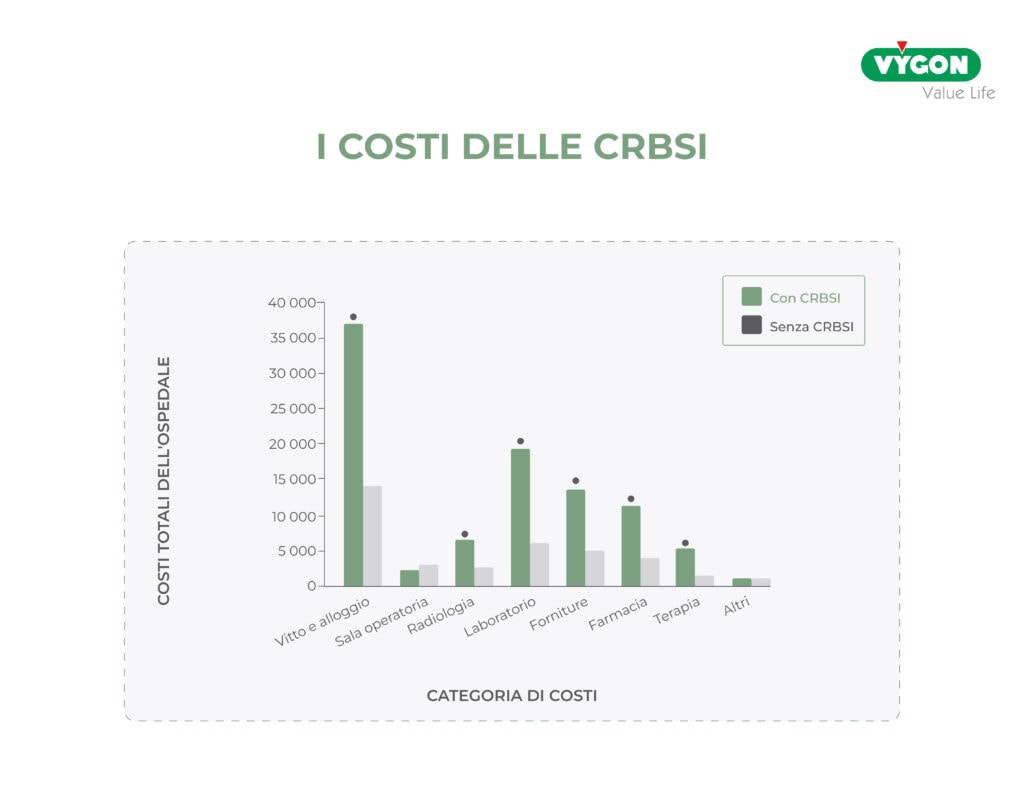
I costi delle CRBSI
Le CRBSI comportano un aumento esponenziale dei costi aziendali per la sostituzione del dispositivo e anche per la durata dell’ospedalizzazione.
Infatti, ogni anno solo nelle Terapie Intensive Italiane si stima che si verifichino 8500 CRBSI che causano un allungamento medio del tempo di degenza di 12,7 giorni ad episodio infettivo con un costo medio per episodio di poco superiore ai 13.000 euro e 1.500 decessi.
Come conseguenza, il Sistema Sanitario Nazionale subisce un aggravio di costi per le sole CRBSI insorgenti nelle Terapie Intensive di oltre 81 milioni di euro.
Secondo alcune indagini, una CRBSI porta ad un aumento del 120% dei costi sostenuti dalla struttura ospedaliera in quanto va ad impattare drammaticamente su tutte le categorie di costi quali la semplice occupazione del letto, l’uso della radiologia, del laboratorio, il consumo di farmaci, ecc.

Obiettivo ‘Targeting zero’
Il progetto del ‘Targeting Zero’ nasce per incoraggiare tutte le istituzioni a eliminare le infezioni nosocomiali (HAI) piuttosto che ad accontentarsi di raggiungere dei semplici valori di riferimento.
I riferimenti alla “Tolleranza zero” oggi si intendono come una risposta a pratiche comportamentali pericolose che pongono sia i pazienti che gli operatori sanitari a rischio.
La cultura della tolleranza zero verso le infezioni nosocomiali e verso tutte le pratiche non sicure è caratterizzata da:
- stabilire l’obiettivo teorico di eliminare le HAI;
- stabilire che le misure per la prevenzione ed il controllo delle infezioni debbano essere applicate costantemente da tutti gli operatori sanitari, nel 100% delle volte;
- un ambiente di lavoro sicuro per gli operatori sanitari cui aderire al 100%, dove essi sono autorizzati a ritenere tutti responsabili della prevenzione delle infezioni;
- sistemi e supporto amministrativo che fornisca la base per implementare con successo le misure preventive;
- trasparenza e apprendimento continuo dove gli errori e/o le défaillance del sistema possano essere discusse apertamente senza timori o punizioni;
- puntuale ricerca delle HAI più temibili per l’organizzazione e/o per la comunità, e focus sulla fornitura di dati in tempo reale al management con l’obiettivo di produrre migliorie.
Il raggiungimento dell’obiettivo ‘Targeting Zero’ si basa sull’adozione di tattiche e strumenti regolati dai cosiddetti “bundles”.
Il concetto di “bundle” (“pacchetto assistenziale”) include un gruppo limitato di interventi (3-5 al massimo) con dimostrata base scientifica, relativi al processo di cura che, quando vengono utilizzati insieme, risultano più efficaci rispetto al loro singolo utilizzo.
A tal proposito, le linee guida internazionali hanno elaborato dei bundles per la prevenzione delle infezioni catetere correlate.
Vuoi saperne di più?
Seguici per il prossimo articolo dedicato ai bundles!
Le infezioni catetere correlate rappresentano dunque un grave problema sia per i pazienti che per gli operatori, andando inoltre ad incidere negativamente sul bilancio del Sistema Sanitario Nazionale.
La strategia di prevenzione si basa su diversi principi come raccomandato dalle linee guida più recenti, i cui capisaldi sono:
- Educazione e training
- Personale dedicato e sufficiente ad espletare la funzione
- Raccomandazioni sull’impianto
- Raccomandazioni sulla gestione
- Formazione specifica di tutti gli operatori sanitari coinvolti in un qualsiasi step di impianto o gestione dell’accesso vascolare
- Formazione dei pazienti sulla gestione del proprio dispositivo
- Utilizzo di bundles
Bibliografia
- American Society of Anesthesiologists Task Force on Central Venous Access, e. (2012). Practice guidelines for central venous access: a report by the American Society of Anesthesiologists Task Force on Central Venous Access. – PubMed – NCBI. [online] Ncbi.nlm.nih.gov.
- American Society of Anesthesiologists, (2020). Practice Guidelines for Central Venous Access 2020.
- ASL Salerno, Presidio Ospedaliero “A. Tortora” Unità di Ematologia ed Oncologia, (2019). Kit procedurali per gestione CVC.
- Blot, S., Poulakou, G. and Timsit, J. (2019). Catheter-associated bloodstream infection rates: how low can you go?.
- Bouza, E., Munoz, P. and Rodriguez, J. (2003). Journal of Hospital Infection | Vol 54, Issue 4, Pages 251-326 (August 2003) | ScienceDirect.com. [online] Sciencedirect.com.
- Burnett, K. (2019). The Impact of Peripheral Venous Catheter Procedural Kits on Improving Clinical Outcomes in Hospitalised Patients. Cdc.gov. (2011). CDC 2011. [online]
- Dimick, J. (2001). Increased Resource Use Associated With Catheter-Related Bloodstream Infection in the Surgical Intensive Care Unit.
- Eggimann, P., Pagani, J., Dupuis-Lozeron, E., MS, B., Thévenin, M., Joseph, C., Revelly, J. and Que, Y. (2019). Sustained reduction of catheter-associated bloodstream infections with enhancement of catheter bundle by chlorhexidine dressings over 11 years. Epidemiologia, Sorveglianza e Promozione della Salute. [online]
- Equivalente.it. (2020). Elaborazioni SIC su dati ISS-ECDC-ASST Emilia Romagna, Dossier 189/2010-MEF 2007. [online]
- Fenik, Y., Celebi, N., Wagner, R., Nikendei, C., Lund, F., Zipfel, S., Riessen, R. and Weyrich, P. (2013). Prepackaged central line kits reduce procedural mistakes during central line insertion: a randomized controlled prospective trial.
- Jointcommission.org. (2015). Central Line Associated Bloodstream Infections Toolkit and Monograph. [online] Available at: https://www.jointcommission.org/resources/patient-safety-topics/infection-prevention-and-control/central-line-associated-bloodstream-infections-toolkit-and-monograph/.
- Kim, J., Holtom, P. and Vigen, C. (2011). Reduction of catheter-related bloodstream infections through the use of a central venous line bundle: Epidemiologic and economic consequences.
- Leppink, J., Gog, T., Paas, F. and Sweller, J. (2015). Cognitive load theory: researching and planning teaching to maximise learning.
- Manuale di formazione per il governo clinico: la sicurezza dei pazienti e degli operatori. Dipartimento della Programmazione e dell’Ordinamento del Servizio Sanitario Nazionale. (2012). Direzione Generale della Programmazione Sanitaria ufficio III.
- Marschall, J. (2014). Strategies to prevent central line-associated bloodstream infections in acute care hospitals: 2014 update. – PubMed – NCBI. [online] Ncbi.nlm.nih.gov.
- Moureau, N. and Dawson, R. (n.d.). Study Finds SwabCap Passively Disinfects IV Needleless Connectors. [online] Infection Control Today.
- New England Journal of Medicine. (2006). An Intervention to Decrease Catheter-Related Bloodstream Infections in the ICU | NEJM. [online]
- O’Grady, N., Alexander, M., Dellinger, E., Gerberding, J., Heard, S., Maki, D., Masur, H., McCormick, R., Mermel, L., Pearson, M., Raad, I., Randolph, A. and Weinstein, R. (2002). Guidelines for the Prevention of Intravascular Catheter–Related Infections.
- Sciencedirect.com. (2008). American Journal of Infection Control | Vol 36, Issue 2, Pages 77-154 (March 2008) | ScienceDirect.com. [online] Available at: https://www.sciencedirect.com/journal/american-journal-of-infection-control/vol/36/issue/2
- Shears, G. (2006). Vascular access device stabilization and line securement – American Nurse. [online] American Nurse.
- Tacconelli, E., Smith, G., Hieke, K., Lafuma, A. and Bastide, P. (2009). Epidemiology, medical outcomes and costs of catheter-related bloodstream infections in intensive care units of four European countries: literature- and registry-based estimates.
- Timsit, J., Schwebel, C., Bouadma, L., Geffroy, A., Garrouste-Orgeas, M., Pease, S., Herault, M., Haouache, H., Calvino-Gunther, S., Gestin, B., Armand-Lefevre, L., Leflon, V., Chaplain, C., Benali, A., Francais, A., Adrie, C., Zahar, J., Thuong, M., Arrault, X., Croize, J., Lucet, J. and Dressing Study Group, f. (2009). Chlorhexidine-Impregnated Sponges and Less Frequent Dressing Changes for Prevention of Catheter-Related Infections in Critically Ill Adults.
- Walz, J., Ellison, R., Mack, D., Flaherty, H., McIlwaine, J., Whyte, K., Landry, K., Baker, S. and Heard, S. (2015). The Bundle “Plus”.
- Wright, M. (2013). American Journal of Infection Control Editorial Board. [online] Journals.elsevier.com. Available at: https://www.journals.elsevier.com/american-journal-of-infection-control//editorial-board.