Il concetto di bundle è stato sviluppato a partire dal 2001 dall’Institute for Healthcare Improvement (IHI) per aiutare gli operatori sanitari ad offrire con maggiore affidabilità la migliore cura a pazienti sottoposti a particolari trattamenti ad alto rischio.
Si cominciò a lavorare con i bundle sui pazienti ricoverati in rianimazione, sottoposti a ventilazione invasiva o portatori di linee centrali. Da allora i bundle sono stati impiegati quali strumenti di miglioramento in diverse specialità mediche e chirurgiche, non più solo in area critica e per le ICA (come la sepsi grave), ma anche per altre condizioni cliniche (come lo scompenso o l’arresto cardiaco in ospedale).
Un “bundle” include un gruppo limitato di interventi (3-5 al massimo) con dimostrata base scientifica relativi al processo di cura che, quando vengono utilizzati insieme, risultano più efficaci rispetto al loro singolo utilizzo.
Particolare fondamentale del bundle è di essere un’unità coesa, organizzata in protocolli, preferibilmente semplici, che consentano una facile misurazione e verifica dell’esecuzione e per il quale vige la legge del “tutto o nulla”, cioè è necessario il completamento di tutti i passaggi per determinare il superamento del bundle.
Come rendere applicabile un bundle procedurale: la checklist
Per poter applicare un bundle bisogna applicare e stendere una checklist, cioè un elenco dettagliato dei punti salienti di ogni singola manovra, allo scopo di verifica in tempo reale della correttezza dell’esecuzione di ciascuna procedura.
Le checklists nascono per rispondere a due difficoltà:
- La prima è la fallibilità della memoria e dell’attenzione umana
- La seconda è la tendenza a saltare alcune operazioni anche quando ci si ricorda che dovrebbero essere eseguite: non tutte le operazioni nella filiera di un processo sono sempre ritenute importanti per cui si prende la scorciatoia, motivata dal fatto che finora non è mai successo niente.
Quindi il bundle serve a favorire la standardizzazione di determinate manovre che hanno dimostrato la loro efficacia per prevenire una determinata complicanza; nel nostro caso le infezioni catetere-correlate.
Per quanto riguarda gli accessi vascolari, le linee guida internazionali suggeriscono l’utilizzo di checklist stilate a partire dai bundles procedurali in modo tale da minimizzare le possibili complicanze (CDC 2011, Epic3 2014, Shea 2014, INS 2021).
Esempio: protocollo Gavecelt 2017 per la prevenzione delle infezioni da dispositivi per accesso venoso.
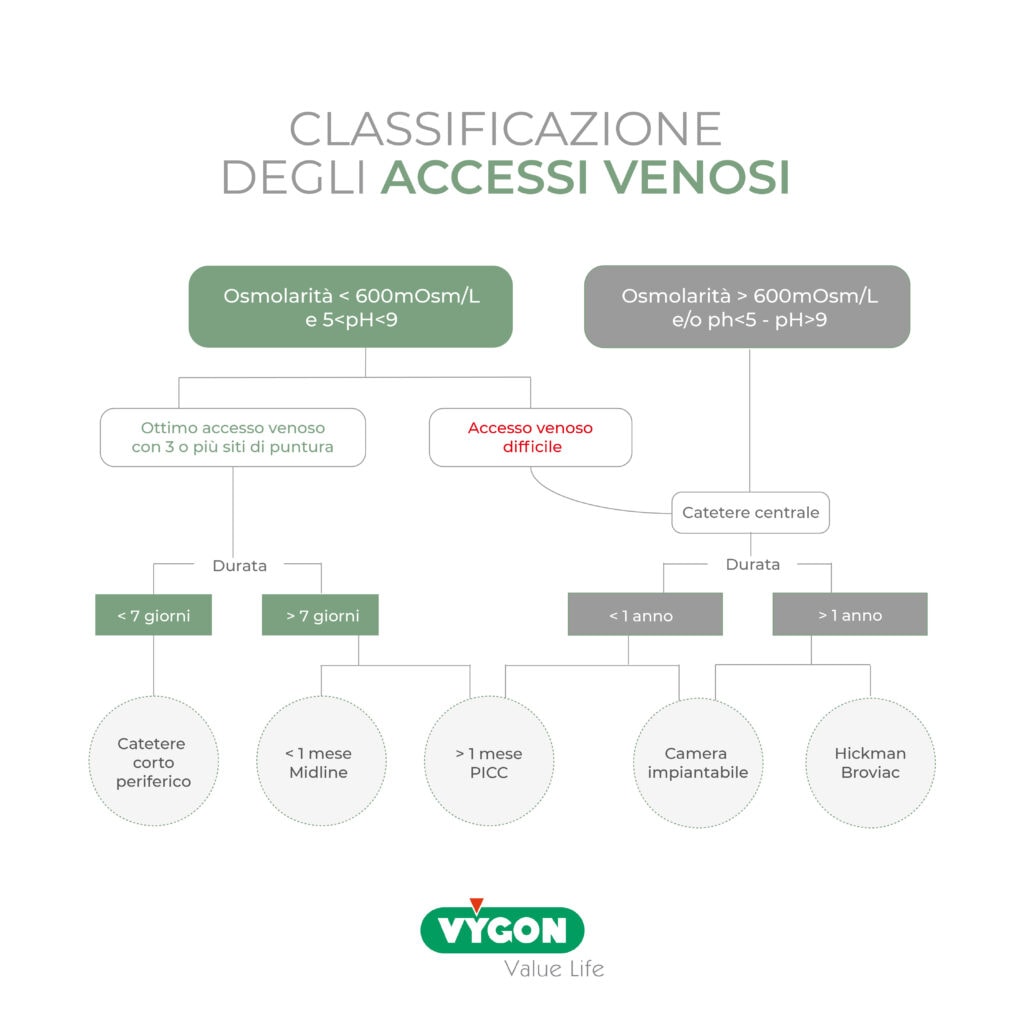
- Corretta indicazione:
verifica dell’indicazione all’accesso venoso, scelta del dispositivo più appropriato (periferico vs. centrale) e sua rimozione appena non è più indispensabile.
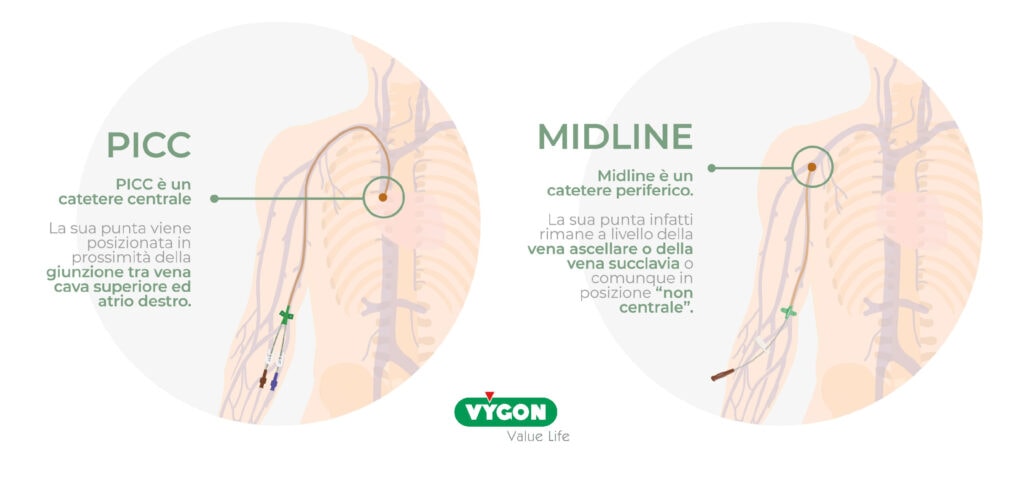
2. Corretta asepsi:
igiene delle mani con gel idroalcolico, prima dell’impianto e prima e dopo ogni manovra di gestione; massime precauzioni di barriera durante l’inserzione di dispositivi per accesso centrale o accesso periferico di lunga durata; antisepsi cutanea con clorexidina 2% in alcool (in applicatori monodose sterili) prima dell’impianto e al momento del cambio della medicazione.
3. Scelta corretta del sito di emergenza:
- Per gli accessi periferici, evitare le zone di flessione;
- Per gli accessi centrali, preferire (nell’ordine) il terzo medio del braccio, la zona sottoclaveare e la zona sopraclaveare; evitare il sito di emergenza al collo o all’inguine (tranne che in urgenza); tunnellizzare un dispositivo per accesso venoso centrale se ciò è necessario ad ottimizzare il sito di emergenza.
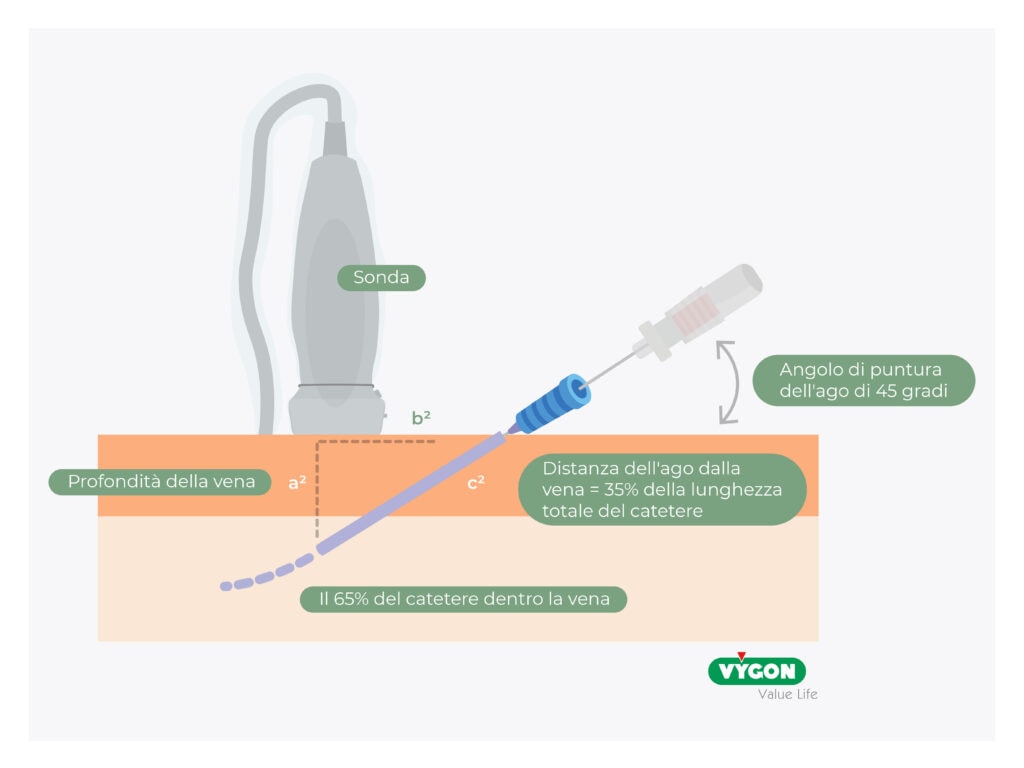
4. Tecnica corretta d’impianto:
utilizzare sempre l’impianto ecoguidato per il posizionamento dei dispositivi centrali e dei dispositivi periferici di media/lunga durata.
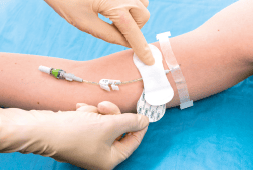
5. Fissaggio appropriato:
evitare sempre punti di sutura e cerotti; stabilizzare invece il dispositivo con un sistema sutureless appropriato.
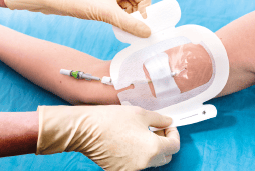
6. Protezione del sito di emergenza:
utilizzare membrane trasparenti semipermeabili ad alta traspirabilità, associate a feltrini a rilascio di clorexidina o a sigillo del sito di emergenza con colla al cianoacrilato.
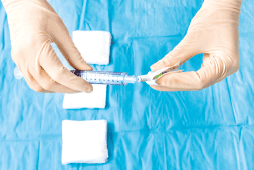
7. Protezione della linea di infusione:
disinfettare le porte di accesso strofinando con soluzioni alcoliche alla clorexidina 2% oppure applicando cappucci disinfettanti sopra ai connettori senz’ago;
- Lavare e chiudere il sistema soltanto con soluzione fisiologica, usando siringhe preriempite sterili.
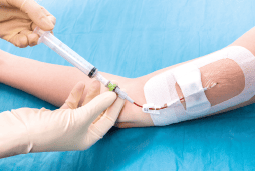
8. Facilitare l’utilizzo dei bundles:
utilizzare carrelli dedicati, kit omnicomprensivi e checklist, sia per l’impianto che per la gestione.
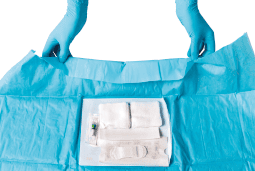
L’importanza di kit preassemblati per l’impianto e la gestione dei dispositivi vascolari
Secondo le attuali indicazioni, l’utilizzo di kit preassemblati è raccomandato nella fase di impianto e gestione per assicurare il successo dei dispositivi vascolari.
Va considerato inoltre il notevole risparmio di tempo da parte del personale che garantisce quindi la corretta attrezzatura, utilizzata per la procedura.
I kit sono assemblati dalle aziende e contengono il materiale raccomandato dalle evidenze; essi possono anche essere personalizzati in base alle esigenze.
Per esempio, un telo chirurgico sterile ampio per la procedura di inserimento, così come clorexidina per antisepsi della cute, maschera e guanti sterili.
Le linee guida per la prevenzione delle infezioni catetere correlate (CDC), indicano l’utilizzo di un carrello che abbia tutto il necessario per l’impianto di catetere venoso centrale (CVC)
Anche l’American Society of Anesthesiologists riporta come raccomandazione l’utilizzo di un kit standard, ribadendo l’utilizzo di un set di strumenti standardizzato per l’impianto di un CVC.
l’INS ugualmente raccomanda l’utilizzo di un carrello o kit standardizzato, contenente tutto il materiale necessario per l’impianto.
Esempio di un kit preassemblato per l’impianto di un catetere venoso centrale:
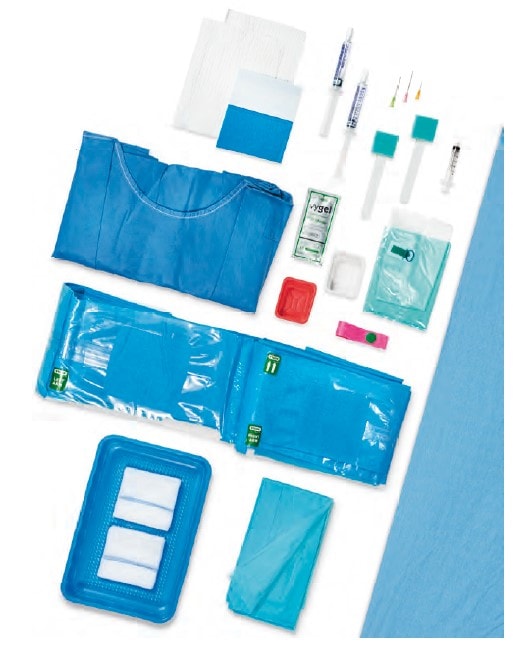
I vantaggi di un kit di inserimento preassemblato
Da uno studio pubblicato dall’Università di Tübigen in Germania, si evidenzia che i kit preassemblati di cateteri venosi centrali potrebbero ridurre significativamente il numero di errori e delle complicanze durante la procedura di impianto.
Lo studio prospettico, controllato e randomizzato in cieco, ha incluso trenta laureati in medicina e studenti di medicina all’ultimo anno, i quali sono stati divisi casualmente in due gruppi composti da quindici persone.
Un gruppo ha posizionato il catetere venoso centrale usando il kit preassemblato con all’interno tutti i componenti necessari mentre il gruppo di controllo ha usato un kit standard contenente solo il catetere e gli elementi compresi nella confezione.
Il secondo gruppo, quindi, ha attivamente selezionato i componenti aggiuntivi necessari per l’impianto dal carrello.
I partecipanti allo studio erano assistiti da studenti di infermieristica ugualmente senza esperienza.
Tutte le procedure sono state video registrate e poi valutate da due medici esperti. La valutazione si è basata su cinquantacinque punti, più cinque indicatori di qualità:
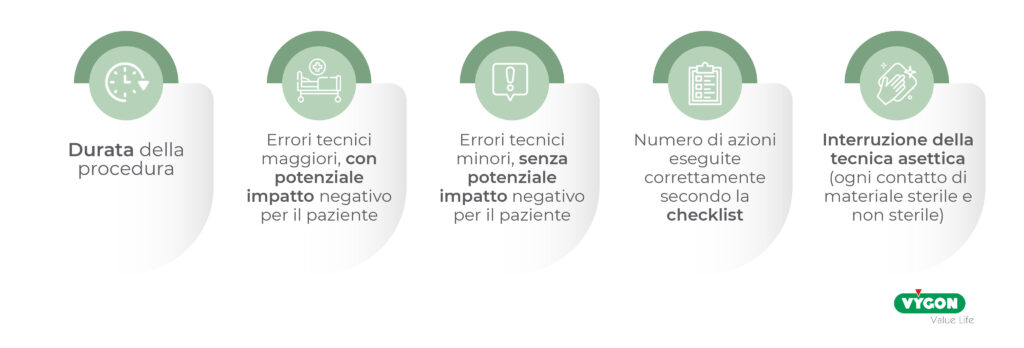
I risultati dello studio hanno dimostrato che il gruppo che aveva utilizzato il kit preassemblato ha fatto il 35% in meno di errori tecnici rispetto al gruppo di controllo, con un maggior rispetto delle sequenze elencate nella checklist. Inoltre, il gruppo del kit preassemblato ha impiegato in media cinque minuti in meno rispetto al gruppo di controllo per eseguire la procedura.
Statisticamente non rilevante, ma degno di nota, la tendenza di una più bassa interruzione della tecnica asettica durante la procedura con il kit.
L’utilizzo di kit preassemblati o pack procedurali dedicati e standardizzati, dunque, aumentano l’affidabilità della procedura, riducendo il tempo necessario per eseguirla, con notevoli benefici della costo/efficacia della procedura stessa e una conseguente riduzione delle complicanze catetere-correlate.
In particolare, i professionisti della salute alle prime armi trarranno beneficio da questi kit in quanto l’impianto di un catetere venoso centrale è una procedura complessa che include vari passaggi e che comporta quindi un importante carico cognitivo.
In accordo con il cosiddetto “principio della divisione dell’attenzione” il carico cognitivo può essere ridotto dall’unione di tante diverse fonti di informazione in una singola fonte.
Da questo principio nascono i kit preassemblati che contengono i componenti necessari per la procedura.
Vuoi saperne di più?
Leggi l’articolo correlato: “Infezioni catetere correlate: impatto sui pazienti e sui costi aziendali”
Bibliografia
- American Society of Anesthesiologists Task Force on Central Venous Access, e. (2012). Practice guidelines for central venous access: a report by the American Society of Anesthesiologists Task Force on Central Venous Access. – PubMed – NCBI. [online] Ncbi.nlm.nih.gov.
- American Society of Anesthesiologists, (2020). Practice Guidelines for Central Venous Access 2020.
- ASL Salerno, Presidio Ospedaliero “A. Tortora” Unità di Ematologia ed Oncologia, (2019). Kit procedurali per gestione CVC.
- Blot, S., Poulakou, G. and Timsit, J. (2019). Catheter-associated bloodstream infection rates: how low can you go?.
- Bouza, E., Munoz, P. and Rodriguez, J. (2003). Journal of Hospital Infection | Vol 54, Issue 4, Pages 251-326 (August 2003) | ScienceDirect.com. [online] Sciencedirect.com.
- Burnett, K. (2019). The Impact of Peripheral Venous Catheter Procedural Kits on Improving Clinical Outcomes in Hospitalised Patients. Cdc.gov. (2011). CDC 2011. [online]
- Dimick, J. (2001). Increased Resource Use Associated With Catheter-Related Bloodstream Infection in the Surgical Intensive Care Unit.
- Eggimann, P., Pagani, J., Dupuis-Lozeron, E., MS, B., Thévenin, M., Joseph, C., Revelly, J. and Que, Y. (2019). Sustained reduction of catheter-associated bloodstream infections with enhancement of catheter bundle by chlorhexidine dressings over 11 years. Epidemiologia, Sorveglianza e Promozione della Salute. [online]
- Equivalente.it. (2020). Elaborazioni SIC su dati ISS-ECDC-ASST Emilia Romagna, Dossier 189/2010-MEF 2007. [online]
- Fenik, Y., Celebi, N., Wagner, R., Nikendei, C., Lund, F., Zipfel, S., Riessen, R. and Weyrich, P. (2013). Prepackaged central line kits reduce procedural mistakes during central line insertion: a randomized controlled prospective trial.
- Jointcommission.org. (2015). Central Line Associated Bloodstream Infections Toolkit and Monograph. [online] Available at: https://www.jointcommission.org/resources/patient-safety-topics/infection-prevention-and-control/central-line-associated-bloodstream-infections-toolkit-and-monograph/.
- Kim, J., Holtom, P. and Vigen, C. (2011). Reduction of catheter-related bloodstream infections through the use of a central venous line bundle: Epidemiologic and economic consequences.
- Leppink, J., Gog, T., Paas, F. and Sweller, J. (2015). Cognitive load theory: researching and planning teaching to maximise learning.
- Manuale di formazione per il governo clinico: la sicurezza dei pazienti e degli operatori. Dipartimento della Programmazione e dell’Ordinamento del Servizio Sanitario Nazionale. (2012). Direzione Generale della Programmazione Sanitaria ufficio III.
- Marschall, J. (2014). Strategies to prevent central line-associated bloodstream infections in acute care hospitals: 2014 update. – PubMed – NCBI. [online] Ncbi.nlm.nih.gov.
- Moureau, N. and Dawson, R. (n.d.). Study Finds SwabCap Passively Disinfects IV Needleless Connectors. [online] Infection Control Today.
- New England Journal of Medicine. (2006). An Intervention to Decrease Catheter-Related Bloodstream Infections in the ICU | NEJM. [online]
- O’Grady, N., Alexander, M., Dellinger, E., Gerberding, J., Heard, S., Maki, D., Masur, H., McCormick, R., Mermel, L., Pearson, M., Raad, I., Randolph, A. and Weinstein, R. (2002). Guidelines for the Prevention of Intravascular Catheter–Related Infections.
- Sciencedirect.com. (2008). American Journal of Infection Control | Vol 36, Issue 2, Pages 77-154 (March 2008) | ScienceDirect.com. [online] Available at: https://www.sciencedirect.com/journal/american-journal-of-infection-control/vol/36/issue/2
- Shears, G. (2006). Vascular access device stabilization and line securement – American Nurse. [online] American Nurse.
- Tacconelli, E., Smith, G., Hieke, K., Lafuma, A. and Bastide, P. (2009). Epidemiology, medical outcomes and costs of catheter-related bloodstream infections in intensive care units of four European countries: literature- and registry-based estimates.
- Timsit, J., Schwebel, C., Bouadma, L., Geffroy, A., Garrouste-Orgeas, M., Pease, S., Herault, M., Haouache, H., Calvino-Gunther, S., Gestin, B., Armand-Lefevre, L., Leflon, V., Chaplain, C., Benali, A., Francais, A., Adrie, C., Zahar, J., Thuong, M., Arrault, X., Croize, J., Lucet, J. and Dressing Study Group, f. (2009). Chlorhexidine-Impregnated Sponges and Less Frequent Dressing Changes for Prevention of Catheter-Related Infections in Critically Ill Adults.
- Walz, J., Ellison, R., Mack, D., Flaherty, H., McIlwaine, J., Whyte, K., Landry, K., Baker, S. and Heard, S. (2015). The Bundle “Plus”.
- Wright, M. (2013). American Journal of Infection Control Editorial Board. [online] Journals.elsevier.com. Available at: https://www.journals.elsevier.com/american-journal-of-infection-control//editorial-board.